
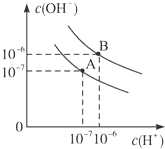
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:| 10-3y-10-4x |
| x+y |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
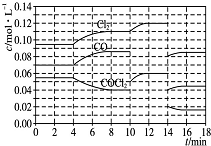 光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.
光气(COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.查看答案和解析>>
科目:高中化学 来源: 题型:
A、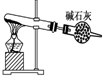 以NH4Cl为原料,如图装置可用于实验室制备少量NH3 |
B、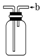 如图装置装满水后由b口进气可收集H2、NO等气体 |
C、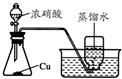 如图装置可用于制取、收集NO2 |
D、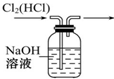 如图装置可用于除去Cl2中的HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、錀 第七周期第ⅠB族 |
| B、镭 第七周期第ⅡA族 |
| C、金 第六周期第ⅠB族 |
| D、鎶 第七周期第ⅡB族 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有① | B、①② |
| C、②④⑤ | D、①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com