
| X | ||||
| Z | W |
| A. | X和氢组成的化合物分子中可能含有极性共价键和非极性共价键 | |
| B. | 工业上用电解Y和W组成的化合物来制备Y | |
| C. | Z、W两元素的气态氢化物中,W的气态氢化物更稳定 | |
| D. | X、Y、Z、W元素最高价氧化物对应的水化物中酸性最强的是HWO4 |
分析 X、Y、Z、W是原子序数依次增大的短周期主族元素,Y是地壳中含量最多的金属元素,则Y为Al;可知Z、W处于第三周期,由元素相对位置可知X处于第二周期,X元素最低负化合价的绝对值与其原子最外层电子数相等,则X为C元素,可推知Z为P元素、W为Cl元素.
解答 解:X、Y、Z、W是原子序数依次增大的短周期主族元素,Y是地壳中含量最多的金属元素,则Y为Al;可知Z、W处于第三周期,由元素相对位置可知X处于第二周期,X元素最低负化合价的绝对值与其原子最外层电子数相等,则X为C元素,可推知Z为P元素、W为Cl元素.
A.X和氢组成的化合物为烃,分子中可能含有极性共价键和非极性共价键,如乙烷等,故A正确;
B.工业上电解熔融氧化铝冶炼Al,故B错误;
C.W的非金属性比Z的强,Z、W两元素的气态氢化物中,W的气态氢化物更稳定,故C正确;
D.X、Y、Z、W元素中Cl元素非金属性最强,最高价氧化物对应的水化物中酸性最强的是HWO4,故D正确.
故选:D.
点评 本题考查结构性质位置关系应用,熟练掌握元素周期表的结构,注意对元素周期律的理解掌握.


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 向水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入二氧化碳气体 | D. | 向水中加醋酸钠晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Ag+、Na+ |
| 阴离子 | NO3-、SO42-、Cl- |
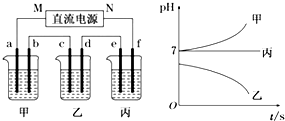
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥⑦ | B. | ①⑤⑦ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中的阳离子只能是金属离子 | |
| B. | 离子化合物中一定含有离子键 | |
| C. | 离子化合物都能溶于水,其水溶液可以导电 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数减小 | |
| B. | 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率增大 | |
| C. | 单位时间内消耗NO和N2的物质的量比为1:1时,反应达到平衡 | |
| D. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
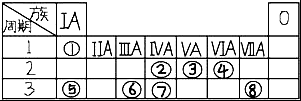 表为元素周期表的一部分,请参照元素①⑧在表中的位置,回答下列问题:
表为元素周期表的一部分,请参照元素①⑧在表中的位置,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核反应发电实现了化学能到电能的转化 | |
| B. | 115 号元素一定是处于VA 族的非金属元素 | |
| C. | 117 号元素与F、Cl、Br、I 均处于VIIA 族 | |
| D. | 四种新元素位于元素周期表中的不同周期 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com