
����Ŀ����(Mo)��һ�ֹ��Ƚ���Ԫ�أ�ͨ�������Ͻ���ֵ����Ӽ��������ƾ��壨Na2MoO42H2O����һ����������ȴˮϵͳ�Ľ�����ʴ������ҵ�������⾫����Ҫ�ɷ��Dz�����ˮ��MoS2���Ʊ������Ƽ��Ʊ����������Ҫ����ͼ��ͼ��ʾ��

��1��Na2MoO4��2H2O����Ԫ�صĻ��ϼ���_______���ᾧ�õ��������ƾ���ʱ�ֲ�Ʒ��Ҫ�õ������������ƾ��壬��һ����Ҫ���еIJ�����___________�������ƣ���
��2�����չ������⾫��������Ҫ��Ӧ�Ļ�ѧ����ʽΪMoS2+O2![]() MoO3+SO2(δ��ƽ)���÷�Ӧ������������__________(�ѧʽ)������Ӧ������36.0gMoO3,��Ӧ��ת�Ƶ��ӵ���ĿΪ__________��
MoO3+SO2(δ��ƽ)���÷�Ӧ������������__________(�ѧʽ)������Ӧ������36.0gMoO3,��Ӧ��ת�Ƶ��ӵ���ĿΪ__________��
��3��β���к���SO2��Ҫ���������в����������ռ�����_______������ţ���
a.Ca(OH)2 b.HNO3 c.Na2CO3
��4������Na2CO3��Һʱ������Ӧ�Ļ�ѧ����ʽΪ_________������߸÷�Ӧ���ʵĴ�ʩ��______������ţ���
a.���ֲ�Ʒ���� b.����̼������Һ��Ũ�� c.�ʵ������¶�
��5���������ȷ�ӦҲ�ɻ��ս����⣬д��MoO3�������ȷ�Ӧ�Ļ�ѧ����ʽ___________��
��6����֪��������Һ��c(MoO42-)=0.40molL-1��c(CO32-)=0.52molL-1������������Һ�Ʊ������ƾ���ʱ�������Ba(OH)2�����Գ�ȥCO32-����BaMoO4��ʼ����ʱ��CO32-��ȥ����Ϊ______��[��֪��Ksp(BaCO3)=2.6��10��9��Ksp(BaMoO4)=4.0��10-8,������Һ������仯]
���𰸡� +6 �ؽᾧ MoO3��SO2 3.5NA b MoO3+Na2CO3=Na2MoO4+CO2�� ac 4Al+2MoO3![]() 2Mo+2Al2O3 95%
2Mo+2Al2O3 95%
����������1������ᾧˮ������������Ԫ�صĻ��ϼ�ֻ����Na2MoO4����Ԫ�صĻ��ϼۼ��ɣ���Ԫ����+1����Ԫ����-2������Ԫ�صĻ��ϼ���x�������ڻ��������������ϼ۴�����Ϊ�㣬��֪����������Ԫ�صĻ��ϼۣ���+1����2+x+��-2����4=0����x=+6���ᾧ�õ��������ƾ����Ǵֲ�Ʒ��Ҫ�õ������������ƾ��壬��һ����Ҫ���еIJ������ؽᾧ����2�����չ������⾫��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��2MoS2+7O2![]() 2MoO3+4SO2��Ԫ�ػ��ϼ����ߵ�ʧȥ���ӷ���������Ӧ�õ����������Ӧ��MoԪ�ػ��ϼ�+2�۱仯Ϊ+6�ۣ���Ԫ�ػ��ϼ�-1�۱仯Ϊ+4�ۣ��÷�Ӧ������������MoO3��SO2����Ӧ������2molMoO3����ת��28mol����Ӧ������36.0gMoO3����0.25molMoO3ʱת�Ƶ��ӵ����ʵ�����28mol/2��0.2��3.5mol����ĿΪ3.5NA����3��SO2����������������������ƻ�̼������Һ��Ӧ��Ҳ�ܱ����������������ɵ�����������Ⱦ��������ѡb����4�����������£�MoO3��Na2CO3��Һ��Ӧ���ɶ�����̼�������ƣ����ӷ���ʽΪMoO3+Na2CO3=Na2MoO4+CO2����a.���ֲ�Ʒ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�a��ȷ��b.����̼������Һ��Ũ�ȷ�Ӧ���ʼ�С��b����c.�ʵ������¶ȣ��ӿ췴Ӧ���ʣ�c��ȷ����ѡac����5��MoO3�������ȷ�Ӧ�Ļ�ѧ����ʽΪ4Al+2MoO3
2MoO3+4SO2��Ԫ�ػ��ϼ����ߵ�ʧȥ���ӷ���������Ӧ�õ����������Ӧ��MoԪ�ػ��ϼ�+2�۱仯Ϊ+6�ۣ���Ԫ�ػ��ϼ�-1�۱仯Ϊ+4�ۣ��÷�Ӧ������������MoO3��SO2����Ӧ������2molMoO3����ת��28mol����Ӧ������36.0gMoO3����0.25molMoO3ʱת�Ƶ��ӵ����ʵ�����28mol/2��0.2��3.5mol����ĿΪ3.5NA����3��SO2����������������������ƻ�̼������Һ��Ӧ��Ҳ�ܱ����������������ɵ�����������Ⱦ��������ѡb����4�����������£�MoO3��Na2CO3��Һ��Ӧ���ɶ�����̼�������ƣ����ӷ���ʽΪMoO3+Na2CO3=Na2MoO4+CO2����a.���ֲ�Ʒ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�a��ȷ��b.����̼������Һ��Ũ�ȷ�Ӧ���ʼ�С��b����c.�ʵ������¶ȣ��ӿ췴Ӧ���ʣ�c��ȷ����ѡac����5��MoO3�������ȷ�Ӧ�Ļ�ѧ����ʽΪ4Al+2MoO3![]() 2Mo+2Al2O3����6����BaMoO4��ʼ����ʱ��Һ�б�����Ũ��c��Ba2+��=Ksp(BaMnO4)/c(MnO4)=Ksp(BaMoO4)/0.4mol/L=1��10��7mol/L����Һ��̼�������Ũ��c��CO32-��=Ksp(BaCO3)/c(Ba2+)��2.6��10��2mol/L������CO32-��ȥ����Ϊ
2Mo+2Al2O3����6����BaMoO4��ʼ����ʱ��Һ�б�����Ũ��c��Ba2+��=Ksp(BaMnO4)/c(MnO4)=Ksp(BaMoO4)/0.4mol/L=1��10��7mol/L����Һ��̼�������Ũ��c��CO32-��=Ksp(BaCO3)/c(Ba2+)��2.6��10��2mol/L������CO32-��ȥ����Ϊ![]() 95%��
95%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±��Ԫ�����������й㷺Ӧ�ã���������֪ʶ�ش��������⡣
��1����Ԫ�ػ�̬ԭ�ӵļ۵����Ų�ͼ��_________��±��Ԫ��λ��Ԫ�����ڱ�______����
��2����һ��Ũ�ȵ��������Һ�У����������Զ����ӵϣ�HF��2��ʽ���ڣ�ʹHF���ӵϵ���������_______________��
��3��BF3�����������壬��ǿ�ҵĽ��ܻ����ӶԵ�����BF3���ӵ����幹��Ϊ______����̬ʱ�ľ���������_______��BF3��NH3�����������ɰ�ɫ���壬д���ð�ɫ�������ʵĽṹʽ����ע�����е���λ��_____��
��4�������±��ṩ�������жϣ��۵���ߡ�Ӳ��������_______���ѧʽ����
���Ӿ��� | NaF | MgF2 | AlF3 |
�����ܣ�KJ��mol-1�� | 923 | 2957 | 5492 |
��5����֪NaClO2������������ΪV�ͣ�ClO2-����ԭ�ӵĻ����Ӷ�����______��ClO2-����ԭ�ӵ��ӻ��������Ϊ_____��HClO4��HClO2����ǿ��ԭ����_______��
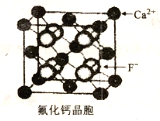
��6��CaF2��������ͼ��ʾ����֪��NAΪ����٤���������������ڵ�����Ca2+�ĺ˼��Ϊacm����CaF2���ܶȿɱ�ʾΪ_____g��cm-3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0��1 mol��L-1CH3COONa��ҺpH =a��������˵����ȷ����
A��CH3COOH�ڳ�����Ka��ֵԼΪl��101-2a
B��Լ��1��0��l0a-14 mol��L-1��ˮ��������
C�����Ⱥ���ҺpH <a
D��������ˮ����ҺpH >a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�����������У������������廯�������_______�����ڷ���������________�����ڱ���ͬϵ�����___________�������ţ�

II����֪ij�л������Է�������Ϊ58���������������ش�
�����л�������ֻ��C��H������л���ķ���ʽΪ______________�������ĺ˴Ź�������ֻ��2���壬�����Ľṹ��ʽΪ______________��__________________��
III�����������������ϵı����Թ��л��ߵķ�ʽ����ϵĶ��������Ϊ�������������� ͼ����ԲϩҲ���ڳ������������ݴ˻ش�

��1����֪��Բϩ��I���ķ���ʽΪC24H12������Բϩ��II���ķ���ʽΪ_______________��
��2��������Բϩ��һ��ȡ������м���ͬ���칹�壺��I����_______�֣���II����_______�֣�
��3������������Բϩ���Ժ�������һ�������·����ӳɷ�Ӧ���ɱ���֬�������������
��������������е�̼ԭ���Ƿ���ͬһƽ���ڣ�______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20 mL 0.01 mol/L CH3COOH��Һ����μ���0.01 mol/L ��NaOH��Һ����Һ��ˮ���������c(H+)�����NaOH��Һ������仯ʾ��ͼ���£�����˵����ȷ����

A. ��a��c���Դ���ĵ�����дٽ�����Ҳ����������
B. b��d������Һ��pH��ͬ
C. e����ʾ��Һ�У�c(Na+)=2c(CH3COO-)��2c(CH3COOH) = 0.01mol/L
D. ��b��d�Ĺ����У��ȴ���pH=7�ĵ�Ҳ����ˮ�����c(H+)=10-7�ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��K2Cr2O7��Һ�д���ƽ�⣺Cr2O72��(��ɫ)+H2O![]() 2CrO42��(��ɫ)+2H+����K2Cr2O7��Һ��������ʵ�飺
2CrO42��(��ɫ)+2H+����K2Cr2O7��Һ��������ʵ�飺
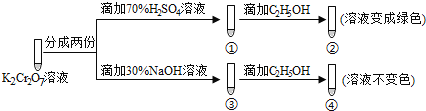
���ʵ�飬����˵������ȷ����
A��������Һ��ɫ���������Һ���
B������Cr2O72����C2H5OH��ԭ
C���Ա���������֪K2Cr2O7������Һ������ǿ
D���������м���70%H2SO4��Һ����������Һ��Ϊ��ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʢ��Ũ��ˮ��ƿ���Ϸ�����һմ���������ʵ������а��̲������ǣ� ��
A. Ũ���� B. Ũ����������Һ C. Ũ���� D. Ũ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǵ�Ԫ����ú��ʹ�ù����е�ת����ϵ��

��1�����м�������ʿ�����___________�����ţ���
a������b��CO c��KNO3d��NH3
��֪��N2(g) +O2(g)=2NO(g) ��H = a kJ��mol-1
N2(g)+3H2(g)=2NH3(g) ��H = b kJ��mol-1
2H2(g)+O2(g)=2H2O(l) ��H = c kJ��mol-1
2CO(g)+O2(g)=2CO2(g) ��H = d kJ��mol-1
����ת����ϵ��Ӧ��ָ������³�ѹ������������Ϣд����������ѡ���ʲ��뷴Ӧ���Ȼ�ѧ����
ʽ___________�������ѡ���ʲ�ֻһ�֣���ֻҪд������һ���Ȼ�ѧ����ʽ���ɣ���
��2���������еĵ�������(NOx)ת��Ϊ�����ʣ�������̳�Ϊ���������淴ӦΪ��������֮һ��
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)��H = -1625.5kJ��mol-1
4N2(g)+6H2O(g)��H = -1625.5kJ��mol-1
������Ӧ����1molN2����Ӧ��ת�Ƶĵ�����Ϊ___________mol��
��ʹ������Ӧ����������ƽ�������ƶ��Ĵ�ʩ��___________��
��������[n(NH3)/n(NO)]��ֱ��Ӱ��÷����������ʡ�350��ʱ��ֻ�ı䰱����Ͷ��������Ӧ��X��ת�����백���ȵĹ�ϵ��ͼ��ʾ����X��___________(�ѧʽ���������Ϊ2L��������ģ�����������Ӧ����ʼʱ����8molNO��3.5molO2��������Ϊ0.5ʱ���÷�Ӧ��ƽ�ⳣ��K =___________��������λС��������n(NH3)/n(NO)>1.0 ʱ��������NOŨ�ȷ���������Ҫԭ����___________���û�ѧ����ʽ��ʾ����

����������Ӧ���������ȵ������н��У���������0.5���ӵ�1.0ʱ���ڴ˹����и÷�Ӧ��ƽ�ⳣ��___________������������������С����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҷ����Ԫ�صļ���ɾ��������ĸ�������ɣ���������ѡ�õ�ʵ����Ʒʹ�ò�ǡ������

A. ����Ҷ���ջһ���ѡ�â١��ڡ��ߺ͢�
B. ��Ũ�����ܽ��Ҷ��������ˮϡ�ͣ�ѡ�âۺ͢�
C. ���˵õ���Һ��ѡ�âܡ��ݺ͢�
D. ��������Һ�е�Fe3+��ѡ�âۡ���͢�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com