
关于NaOH溶液和Fe(OH)3胶体描述正确的是
A.两者的分散质都属于碱
B.两者均为有色不透明的分散系
C.两者分散质的直径都介于10-9~10- 7m之间
D.一束光线分别通过时,两者都会产生“丁达尔效应”
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.Cu溶于稀硝酸HNO3:Cu+2H++NO3-=Cu2++NO2↑+H2O
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓
C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O=Al(OH) 3↓+HCO3-
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
在0.1 mol·Lˉ1醋酸溶液中加入少量0.1 mol·Lˉ1盐酸,下列叙述正确的是 ( )
A.CH3COOH的电离度减小,pH减小
B.平衡向生成CH3COOH方向移动,c(H+)减小
C.CH3COOH的电离度增大,c(H+)增大
D.电离平衡向生成CH3COOˉ、H+方向移动,pH减小
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:填空题
有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I-、NO3-、CO32-、SO42-、AlO2-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除__________的存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除____ __的存在。
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液由酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除________的存在。
(4)取出部分(3)中的碱性溶液加入Na2CO3溶液,有白色沉淀生成,证明有________的存在,可以排除_____的存在。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是
A.使红色布条退色(HCl)
B.滴加AgNO3溶液生成白色沉淀(Cl-)
C.将NaHCO3固体加入新制氯水中,有无色气泡(H+)
D.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是
A.用小苏打治疗胃酸过多: HCO3- + H+ == CO2↑+ H2O
B.往碳酸镁中滴加稀盐酸: CO32- + 2H+ == CO2↑+ H2O
C.往氨水中滴加氯化铝: Al3+ + 4OH- == AlO2- + 2H2O
D.氢氧化钡溶液与稀硫酸反应: Ba2+ + SO42- + H+ + OH- == BaSO4↓+ H2O
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第二次质量检查化学试卷(解析版) 题型:选择题
O、Si、Al是地壳中含量最多的三种元素,Na、Mg、Cl是海水中的重要元素。下列说法正确的是
A.普通玻璃、水泥成分中都含有O、Si、Al三种元素
B.从海水中制备Na、Mg、Al三种元素单质的反应都是氧化还原反应
C.电解熔融状态的SiO2、Al2O3可以制得Si、Al,且都有氧气生成
D.加热蒸干NaCl、MgCl2溶液时可以得到晶体NaCl、MgCl2
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:填空题
(6分)开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有______个。
②LiBH4由Li+和BH4-构成,BH4 -呈正四面体构型。LiBH4中不存在的作用力有______(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为______。
(2) 金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
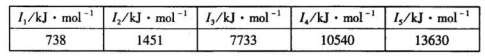
M是______(填元素符号)。
(3)某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有______种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com