
【题目】下列各项叙述中,正确的是
A.AB3型的分子空间构型一定为平面三角形
B.电负性相差越大的元素间越易形成离子键
C.分子晶体中,分子间作用力越大,分子越稳定
D.用于幽门螺旋杆菌示踪的![]() 价电子排布为2s22p3
价电子排布为2s22p3
科目:高中化学 来源: 题型:
【题目】常温下,下列说法错误的是( )
A. c(H+)为1.0×10-4mol·L-1的醋酸溶液的pH=4
B. 0.1 mol·L-1某酸溶液的pH=1
C. 0.01 mol·L-1氨水的pH<12
D. pH=3的醋酸溶液的浓度大于1.0×10-3mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3![]() NH4++NH2-据此判断以下叙述错误的是
NH4++NH2-据此判断以下叙述错误的是
A. 液氨中含有NH3、NH4、NH2-三种微粒
B. 一定温度下液氨中c(NH4+)·c(NH2-)是一个常数
C. 液氨的电离达到平衡c(NH3)= c(NH4+)=c(NH2-)
D. 只要不加入其他物质,液氨中c(NH4+)=c(NH2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH 与微粒浓度的变化关系如图所示。 下列说法错误的是( )
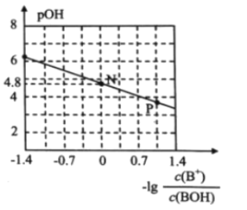
A.若向0.1mol/L BOH溶液中加水稀释,则溶液中c(OH-)/c(BOH) 增大
B.室温下,BOH的电离平衡常数K = 1×10-4.8
C.P点所示的溶液中:c(Cl-) > c(B+)
D.N点所示的溶液中: c(H+) = c(Cl-) + c(OH-) - c(BOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香化合物A(C9H9O3Br)可以发生如图所示的转化,合成两种重要的高分子化合物G和H(其他产物和水已略去)。
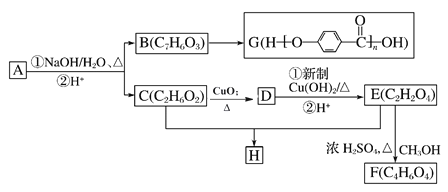
已知A遇氯化铁溶液显紫色,请回答下列问题:
(1)B的结构简式为____________,其核磁共振氢谱图显示有______种不同环境的氢原子。
(2)D的名称是________________;C和E生成H的反应类型为 _______________
(3)1molA与足量NaOH 溶液充分反应,消耗NaOH的物质的量为____________
(4)C生成D的化学方程式为________________________
(5)W是B的同系物,比B多一个碳原子, 符合下列条件的W的同分异构体有______种。
①遇氯化铁溶液显紫色
②既能发生水解反应又能发生银镜反应
(6)参照上述合成路线,根据信息,以乙醇为原料(无机试剂任选)设计制备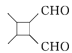 的合成路线_______________
的合成路线_______________
ⅰ.![]()
![]()
![]() +H2O(R1、R2为烃基或氢)
+H2O(R1、R2为烃基或氢)
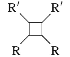
ⅱ.R-HC![]() CH-R'
CH-R'![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不属于电离方程式的是( )。
A.2H2O ![]() H3O++OH-B.CH3COOH+H2O
H3O++OH-B.CH3COOH+H2O ![]() CH3COO-+H3O+
CH3COO-+H3O+
C.H2CO3![]() H++HCO3-D.CH3COOH+NaOH = CH3COONa+H2O
H++HCO3-D.CH3COOH+NaOH = CH3COONa+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为:正极:_____________________________ ;负极:______________________。
(2)为了降低某水库铁闸门被腐蚀的速率,可以采用甲图所示的方案,其中焊接在闸 门上的固体材料R可以采用___________。
A.铜 B.钠 C.锌 D.石墨
(3)乙图所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的___________极。

(4)铅蓄电池是化学电源,其电极材料分别为Pb和PbO2,电解质溶液为稀硫酸,放电时电池的总反应为Pb + PbO2 + 2H2SO4== 2PbSO4 + 2H2O。根据上述情况判断:
①铅蓄电池的正极材料是_______(填“Pb”或“PbO2”),负极的电极反应式为_______________________________________。
②铅蓄电池工作时,电解质溶液中SO42﹣移向________极(填“负”或“正”),溶液的pH___________ (填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g)![]() CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )
CH3OH(g)反应过程中的能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是( )

A.该反应的ΔH=+91 kJ·mol-1
B.加入催化剂,该反应的ΔH变小
C.反应物的总能量大于生成物的总能量
D.如果该反应生成液态CH3OH,则ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 X(g)+Y(g) ![]() 2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
2Z(g) △H<0,在一定条件下,反应情况如图所示.若使曲线b变为曲线a可采取的措施是
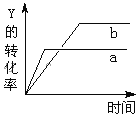
A.加入催化剂B.增大压强
C.升高温度D.保持容器体积不变,冲入He气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com