
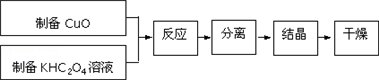
分析 (1)①过滤一般在漏斗中进行,且用玻璃棒引流,用烧杯盛装滤液;
②CuO表面会附着硫酸根离子,用氯化钡溶液检验最后一次洗涤液中是否含有硫酸根离子判断是否洗涤干净;
(2)①提高氧化铜的利用率,可用氧化铜与KHC2O4溶液充分反应;
②CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O;
(3)从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,可用加入少量乙醇,并用蒸馏的方法分离乙醇.
解答 解:(1)①过滤装置所需的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:漏斗、烧杯、玻璃棒;
②CuO表面会附着硫酸根离子,检验是否洗涤干净的具体方法是:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净,
故答案为:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净;
(2)①过滤时滤纸上沾有大量的氧化铜固体,所以应直接将洗涤干净的氧化铜固体连同滤纸一起加入到草酸氢钾溶液中,充分反应后取出滤纸或将滤纸灼烧成灰再将剩余的固体转入热的KHC2O4溶液,
故答案为:ad;
②根据题意可知,CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O,反应的方程式为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O,
故答案为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O;
(3)①从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,降低硫酸铜的溶解度,有利于硫酸铜晶体析出,可用加入少量乙醇,
故答案为:降低硫酸铜的溶解度,有利于硫酸铜晶体析出;
②在蒸发浓缩的初始阶段还采用了蒸馏的方法,可起到回收乙醇的作用,故答案为:回收乙醇.
点评 本题考查物质的制备,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的原理和操作,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3COOH | B. | CH3COOCH2CH3 | C. | CH2=CHCOOH | D. | 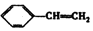 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 11.72 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为20的氯原子:${\;}_{17}^{37}$Cl | |
| B. | 次氯酸的电子式: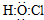 | |
| C. | 氮原子的结构示意图: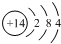 | |
| D. | 碳酸氢钠的电离方程式:NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
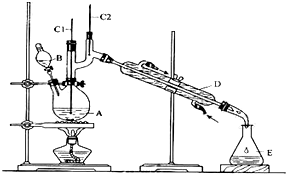
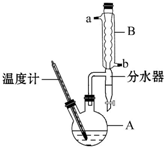 1-溴丙烷常用作有机反应的溶剂.实验室制备1-溴丙烷(CH3CH2CH2Br)的反应和主要实验装置如图:
1-溴丙烷常用作有机反应的溶剂.实验室制备1-溴丙烷(CH3CH2CH2Br)的反应和主要实验装置如图:| 相对分 子质量 | 密度 /g•mL-1 | 沸点/℃ | 水中 溶解性 | |
| 正丙醇 | 60 | 0.896 | 97.1 | 溶 |
| 正丙醚 | 102 | 0.74 | 90 | 几乎不溶 |
| 1-溴丙烷 | 123 | 1.36 | 71 | 不溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
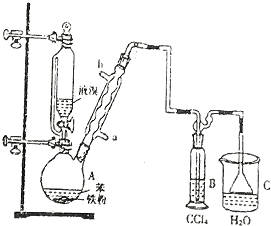
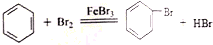 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应前后气体的压强之比为2:1 | |
| B. | 反应前后气体的密度之比为15:16 | |
| C. | 此时CO的转化率为50% | |
| D. | 如果反应继续向正向进行,气体的平均相对分子质量将减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com