
��14�֣���һ�ܱ������г���1molH2��1molI2��ѹǿΪp��Pa��������һ���¶���ʹ������Ӧ��I2(g) + H2(g) 2HI(g) ��H��0��
2HI(g) ��H��0��
��1�����������ݻ����䣬�����м���1molH2����Ӧ���� �����������С�����䡱����ͬ�������������ݻ����䣬�����м���1molN2��N2���μӷ�Ӧ������Ӧ���� ��
��2����������������ѹǿ���䣬�����м���1molN2��N2���μӷ�Ӧ������Ӧ���� ����������������ѹǿ���䣬�����м���1molH2(g)��1molI2(g)����Ӧ���� ��
��3�����������Ϊ10L����Ӧ��ƽ��ʱ�����c(H2)=0.08mol/L����÷�Ӧ��ƽ�ⳣ��K= ��
��4���������¶��£���10L��������ͨ��H2��I2������2mol����ﵽƽ��ʱc (H2)= ��
��1������(2��)������(2��)����2����С(2��)������(2��)����3��0.25(3��)����4��0.16mol/L(3��)��
��������
�����������1�����������ݻ����䣬�����м���1molH2���������˷�Ӧ���Ũ�ȣ���Ӧ���������������ݻ����䣬�����м���1molN2������N2���μӷ�Ӧ�����Է�Ӧ���Ũ�Ȳ��䣬��˷�Ӧ���ʲ��䣻��2����������������ѹǿ���䣬�����м���1molN2����ΪN2���μӷ�Ӧ���������ݻ������ڷ�Ӧ����˵��Ũ�ȼ�С�����Ի�ѧ��Ӧ���ʼ�С����������������ѹǿ���䣬�����м���1molH2(g)��1molI2(g)�����ڷ�Ӧ���Ũ�Ȳ��䣬���Ի�ѧ��Ӧ����Ҳ���䣻��3�����������Ϊ10L����Ӧ��ƽ��ʱ�����c(H2)=0.08mol/L����c(I2)=0.08mol/L; c(HI)=0.04mol/L,���Ը÷�Ӧ��ƽ�ⳣ��K=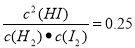 ����4�������¶Ȳ��䣬���Ի�ѧƽ�ⳣ���Ͳ��䣬���¶��£���10L��������ͨ��H2��I2������2mol������ﵽƽ��ʱH2��Ũ����x,��ﵽƽ��ʱK=
����4�������¶Ȳ��䣬���Ի�ѧƽ�ⳣ���Ͳ��䣬���¶��£���10L��������ͨ��H2��I2������2mol������ﵽƽ��ʱH2��Ũ����x,��ﵽƽ��ʱK=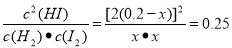 ,���x=c (H2)= 0.16mol/L��
,���x=c (H2)= 0.16mol/L��
���㣺���黯ѧ��Ӧ���ʵ�Ӱ�����ء��Ƚϼ���ͻ�ѧƽ�ⳣ���ļ�����Ӧ�õ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�����ij�ص���ѧͬ����ҵ������1�ս̰棩2.1������ԭ��Ӧ ���ͣ�ѡ����
��ͭ�̡�����ͭ�⣬���Ļ�ѧ�ɷ���Cu2(OH)2CO3(��ʽ̼��ͭ)��ͭ�ڳ�ʪ�Ŀ���������Ļ�ѧ��ӦΪ2Cu+O2+CO2+H2O====Cu2(OH)2CO3�������йظ÷�Ӧ��˵����ȷ���ǡ�(����)
A���÷�Ӧ����������ԭ��Ӧ
B���÷�Ӧ����Ԫ�غ�̼Ԫ�ػ��ϼ۷����仯��������������ԭ��Ӧ
C���÷�Ӧ��ͭ�õ��ӣ�O2ʧ���ӣ�������������ԭ��Ӧ
D���÷�Ӧ��������ԭ��Ӧ����۵�ֻ������Ԫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�߶����ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ������
(8��)��25 ��ʱ����pHΪx�������pHΪy��NaOH��Һ��ȡVx L������ͬ��NaOH��Һ�кͣ���Vy L NaOH��Һ���ʣ�
��1����x��y��14��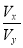 ��___________(����ֵ)��
��___________(����ֵ)��
��2����x��y��13��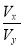 ��__________(����ֵ)��
��__________(����ֵ)��
��3����x��y>14��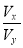 ��____________________________________(����ʽ)��
��____________________________________(����ʽ)��
��Vx________Vy(�>������<������)(����x��6��y��8)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�߶����ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������л�ѧ����������ͬ���ǣ� ��
A��HCl MgCl2 NH4Cl B��H2O Na2O CO2
C��CaCl2 NaOH H2S D�� NH3 H2O CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�������ʡ�߶����ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Ӧ��A B + C �������²����Է����У��ڸ��������Է����У��Ը÷�Ӧ���̡�H����S���ж���ȷ���ǣ� ��
B + C �������²����Է����У��ڸ��������Է����У��Ը÷�Ӧ���̡�H����S���ж���ȷ���ǣ� ��
A����H��0����S��0 B����H��0����S��0
C����H��0����S��0 D����H��������S��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��B�ࣩ�Ծ��������棩 ���ͣ�ѡ����
������ʵ��������ɳ����ԭ�����͵���( )
A����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ����
B������ѹǿ��������SO2��O2��Ӧ����SO3
C�����ű���ʳ��ˮ���ռ�Cl2
D����ҵ��ȡ������Na(l)+ KCl(l)  NaCl(l)+ K(g)ѡ���˵��¶ȣ�ʹK�������ӷ�Ӧ������з������
NaCl(l)+ K(g)ѡ���˵��¶ȣ�ʹK�������ӷ�Ӧ������з������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��B�ࣩ�Ծ��������棩 ���ͣ�ѡ����
SF6��һ�������ľ�Ե���壬���ӽṹ��ֻ����S-F������֪��1molS(s)ת��Ϊ��̬��ԭ����������280 kJ,����1molF-F ��S-F�������յ������ֱ�Ϊ160 kJ��330 kJ����S(s)��3F2(g)��SF6(g)�ķ�Ӧ�ȡ�HΪ
A��-1780kJ/mol B��-1220 kJ/mol C��-450 kJ/mol D��+430 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������������ϸ���ѧ�߶���㿼�Ի�ѧ��A�ࣩ�Ծ��������棩 ���ͣ�ѡ����
������ijУʵ��С����Ƶ�һ��ԭ���װ�ã������й���������ȷ����(����)
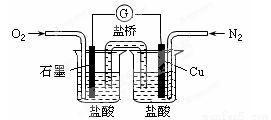
A����װ���ܽ���ѧ��ת��Ϊ����
B��ʯī�缫�ķ�Ӧʽ��O2+2H2O+4e��=4OH��
C��������Cu�缫����������ʯī�缫
D������ܵķ�Ӧ�ǣ�2Cu+O2+4HCl=2CuCl2+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ���Ȼ�菉���ľ�������֪������2�������Cl- ���Ӻ˼��Ϊa cm���Ȼ�蘆�Ħ������ΪM g��mol��NAΪ�����ӵ����������Ȼ�菉�����ܶ�Ϊ�� ��
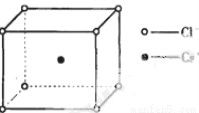
A��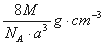 B��
B��
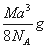
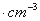
C�� 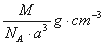 D��
D�� 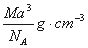
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com