
【题目】粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.进行如下实验: ①取适量A进行铝热反应,产物中有单质B生成;
②另取20g A全部溶于0.15L 6.0mol盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出 l.12L(标况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色.请填空:
(1)①中引发铝热反应的实验操作 , 产物中的单质B是 .
(2)②中所发生的各反应的化学方程式是
(3)③中所发生的各反应的离子方程式是 .
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为 , c(Fe2+)为 .
【答案】
(1)加少量KClO3,插上镁条并将其点燃; Fe
(2)MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O
(3)Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+
(4)0.67mol/L;2.33mol/L
【解析】解:①铝热反应本质是置换反应,金属性Al>Fe,所以发生Al与Fe2O3反应,置换出铁,即B为Fe;
②MgO与盐酸反应生成氯化镁与水,Fe2O3与盐酸反应生成氯化铁与水,溶液C中含有MgCl2、FeCl3;
③单质B和溶液C反应,放出1.12L(标准状况)气体,说明生成氢气,说明②中盐酸过量,溶液C为MgCl2、FeCl3、HCl混合溶液,反应同时生成溶液D,还残留有固体物质B,说明Fe有剩余,结合④用KSCN溶液检验时,溶液D不变色,说明D溶液不含铁离子,则D中溶质为MgCl2、FeCl2.(1)①中引发铝热反应操作为:加少量KClO3,插上镁条并将其点燃,产物中的单质B是Fe,
所以答案是:加少量KClO3,插上镁条并将其点燃;Fe;(2)氧化镁与盐酸反应生成氯化镁与水,氧化铁与盐酸反应生成氯化铁与水,反应方程式为:MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O,
所以答案是:MgO+2HCl=MgCl2+H2O、Fe2O3+6HCl=2FeCl3+3H2O;(3)Fe与盐酸反应生成氯化亚铁与氢气,反应离子方程式为:Fe+2H+=Fe2++H2↑,铁与氯化铁反应生成氯化亚铁,反应离子方程式为Fe+2Fe3+=3Fe2+,
所以答案是:Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+;(4)令MgO和Fe2O3的物质的量分别为xmol,则40x+160x=20,解得x=0.1,溶液D为MgCl2、FeCl2的混合溶液,根据镁元素守恒可知,n(Mg2+)=n(MgO)=0.1mol,所以c(Mg2+)= ![]() =0.67mol/L;根据电荷守恒溶液中2c(Mg2+)+2c(Fe2+)=c(Cl﹣),所以2×0.67mol/L+2c(Fe2+)=6mol/L,解得c(Fe2+)=2.33mol/L,
=0.67mol/L;根据电荷守恒溶液中2c(Mg2+)+2c(Fe2+)=c(Cl﹣),所以2×0.67mol/L+2c(Fe2+)=6mol/L,解得c(Fe2+)=2.33mol/L,
所以答案是:0.67mol/L;2.33mol/L.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知烯烃在酸性KMnO4溶液中双键断裂形式为: 
![]()

现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2﹣COOH,由此推断此二烯可能的结构简式为( )
A.(CH3)2C═C(CH3)CH2CH2CH═CH CH2CH3
B.(CH3)2C═CHCH2CH2C(CH3)═CHCH3
C.CH3CH═C(CH3)CH2CH2CH2C(CH3)═CH2
D.CH3CH═C(CH3)CH2CH2CH2CH═CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如图所示装置进行石油分馏的实验. 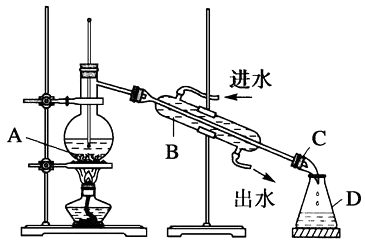
(1)指出实验装置中仪器A、B、C、D的名称: A、B、C、D .
(2)指出该同学所设计的实验装置中存在的错误,并给予改正. 错误:①;② .
改正:①;②
(3)实验装置改正后,进行气密性检查的方法: .
(4)蒸馏烧瓶中放入几片碎瓷片的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有硅酸钠、石灰石、二氧化硅三种白色粉末,只用一种试剂就可以将它们鉴别开,该试剂是( )
A. 纯水 B. 盐酸 C. 硝酸银溶液 D. 碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将煤块粉碎、经脱硫处理、在适当过量的空气中燃烧, 这样处理的目的是:
①使煤充分燃烧, 提高煤的利用率
②减少SO2的产生,避免造成“酸雨”
③减少有毒的CO产生, 避免污染空气
④减少CO2的产生,避免“温室效应”
A. ①②③ B. ②③④
C. ①③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四种元素中,其单质还原性最强的是
A.基态原子最外电子层排布为2s22p5的元素
B.基态原子最外电子层排布为3s1的元素
C.原子核外电子数最少的元素
D.第二周期中基态原子含有未成对电子最多的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用反应2C+SiO2 ![]() Si+2CO↑冶炼硅单质,有关叙述错误的是( )
Si+2CO↑冶炼硅单质,有关叙述错误的是( )
A.每当固体质量减轻5.6g时,生成2.8g Si
B.氧化剂和还原剂的物质的量之比为1:2
C.硅单质在常温下不与任何酸、碱反应
D.单质硅与单质碳均具有一定的还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com