
【题目】如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。

根据图示回答问题:
(1)写出下列物质的化学式: C ,E ,I ,J 。
(2)反应①的离子方程式是_____________________;反应②的化学方程式是________________________;
(3)F与I反应的离子方程式是__________________;
(4)向一定体积的稀硫酸中加入少量的J固体,反应后的溶液与NaClO发生氧化还原反应的离子方程式是_______________。
【答案】(1)NaOH;Al2O3;AlCl3 ;Fe3O4;
(2)2Al+2OH-+2H2O=2AlO2-+3H2↑;3Fe+4H2O(g) ![]() Fe3O4+4H2
Fe3O4+4H2
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓
(4)2Fe2++ClO-+2H+=2Fe3++H2O+Cl-
【解析】
试题分析:B是地壳中含量最高的金属元素,则B为Al,H与D在高温下得到G、J,G是气体,J是磁性材料,常温下H为无色液体,该转化为Fe+H2O![]() Fe3O4+H2,故D为Fe,H为H2O,J为Fe3O4,G为H2,故A与B的反应为铝热反应,则A为Fe2O3,E为Al2O3;由反应①Al+C→F+H2,C为酸或碱,F为铝盐或偏铝酸盐,由F与I相互可知,F为NaAlO2,I为AlCl3,故C为NaOH。
Fe3O4+H2,故D为Fe,H为H2O,J为Fe3O4,G为H2,故A与B的反应为铝热反应,则A为Fe2O3,E为Al2O3;由反应①Al+C→F+H2,C为酸或碱,F为铝盐或偏铝酸盐,由F与I相互可知,F为NaAlO2,I为AlCl3,故C为NaOH。
(1)由上述分析可知,C为NaOH,E为Al2O3,I为AlCl3,J为Fe3O4,故答案为:NaOH;Al2O3;AlCl3 ;Fe3O4;
(2)反应①是铝与氢氧化钠反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,反应②的化学方程式为:3Fe+4H2O![]() Fe3O4+4H2, 2Al+2OH-+2H2O═2AlO2-+3H2↑;3Fe+4H2O
Fe3O4+4H2, 2Al+2OH-+2H2O═2AlO2-+3H2↑;3Fe+4H2O![]() Fe3O4+4H2;
Fe3O4+4H2;
(3)F与I反应的离子方程式是为,故答案为:Al3++3AlO2-+6H2O===4Al(OH)3↓;
(4)J为Fe3O4与稀硫酸反应生成硫酸亚铁和硫酸铁,硫酸亚铁与NaClO发生氧化还原反应生成硫酸铁和氯化钠,反应的离子方程式是2Fe2++ClO-+2H+===2Fe3++H2O+Cl-,故答案为:2Fe2++ClO-+2H+===2Fe3++H2O+Cl-。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和硝酸银用棕色试剂瓶保存
B.常温下铁和铂都不溶于浓硝酸
C.亚硫酸盐和硫酸亚铁固体长期暴露在空气中变质
D.H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
键能/(kJmol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是 。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是 。
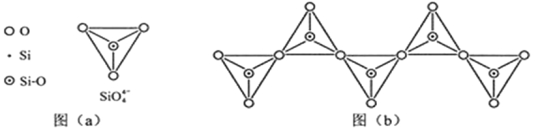
(6)在硅酸盐中,SiO4- 4四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为 ,Si与O的原子数之比为 ,化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法存在安全隐患或导致实验失败的是
A. 将1mol·L-1FeCl3溶液滴入沸水中制备Fe(OH)3胶体
B. 氢气还原氧化铜实验中,先通氢气后加热氧化铜
C. 将FeCl3稀溶液加热蒸发浓缩制备FeCl3浓溶液中
D. 用烧瓶加热液体时投入碎瓷片以防暴沸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物CxHmOn完全燃烧时需要氧气的物质的量是该有机物的x倍,则其化学式中x、m、n的关系不可能的是 ( )
A.m︰n=2︰1 B.m=2x+2 C.x︰m︰n=1︰2︰1 D.m>2x+2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是( )
A.![]() N2H4(g)+
N2H4(g)+![]() O2(g)===
O2(g)===![]() N2(g)+H2O(g) ΔH=+267 kJ·mol-1
N2(g)+H2O(g) ΔH=+267 kJ·mol-1
B.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-133.5 kJ·mol-1
C.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=+534 kJ·mol-1
D.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将淀粉与KCl的混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是
A.加入碘水不变色 B.加入AgNO3 溶液产生白色沉淀
C.加入AgNO3 溶液不产生白色沉淀 D.加入碘水变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Fe2+ 、Mg2+、Cu2+、NH4+、Al3+。当加入1 种淡黄色固体并加热时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出的沉淀和产生气体的物质的量(纵坐标)的关系如图所示。
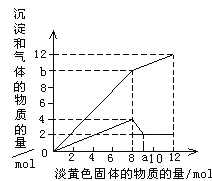
(1)淡黄色固体是__________________________。
(2)可知溶液中一定没有的离子是 ,理由是 。
(3)请解释为什么在投入8mol淡黄色固体后,产生气体的量在减少 。
(4)写出淡黄色固体加入的量为8mol到10mol之间发生的所有离子方程式 。
(5)所含离子的物质的量之比为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢(H2S)的转化是资源利用和环境保护的重要研究课题。
(1)H2S和CO混合加热可制得羰基硫(COS)。羰基硫可作粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。反应方程式为:
CO(g)+H2S(g)![]() COS(g)+H2(g)
COS(g)+H2(g)
①羰基硫的电子式为_________其含有的共价键类型是________共价键。
②下列能说明碳与硫两元素非金属性相对强弱的是_____________。
a.相同条件下水溶液的pH:Na2CO3 > Na2SO4
b.酸性:H2SO3 > H2CO3
c.S与H2的化合比C与H2的化合更容易
(2)H2S具有还原性,在酸性条件下,能与KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式__________________。
(3)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。
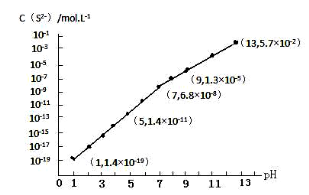
①pH=13时,溶液中的c(H2S)+c(HS-)=____________mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=____________时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]。
(4)H2S的废气可用烧碱溶液吸收,将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:
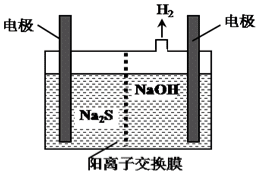
S2--2e-=S↓ (n-1)S+S2-![]() Sn2-
Sn2-
①写出电解时阴极的电极反应式:______________________。
②Na2S溶液中离子浓度由大到小顺序:________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com