
90℃时水的离子积KW=3.8×10-13 m ol2·L-2,该温度时纯水的pH是( )
ol2·L-2,该温度时纯水的pH是( )
A.等于7 B.小于7
C.大于7 D.无法确定
科目:高中化学 来源: 题型:
(1)下列说法不正确的是________(填字母)。
A.60周年国庆阅兵车HQE顶级红旗采用全铝车身,铝的氧化物属于碱性氧化物
B.用热的纯碱溶液洗涤沾有油污的器具时发生的主要是化学变化
C.英国华裔科学家高锟因在“光在纤维中的传输应用于光学通信方面”做出了突破性成就,而获得了2009年诺贝尔物理学奖,光纤制品的基本原料为SiO2
D.液氨、液氯、液态氯化氢都是非电解质
E.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
F.化学变化前后原子的种类、数目不变,分子数目也不变
(2)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深,由低级到高级的认识过程。
①1887年阿仑尼乌斯提出电离理论。
②1923年丹麦化学家布朗斯特和英国化学家劳莱提出了质子论:凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论,下列粒子的水溶液既可看作酸又可看作碱的是________(填字母)。
A.H2O B.NH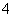 C.OH- D.HCO
C.OH- D.HCO
E.CH3COO- F.Cl-
③1923年路易斯(Lewis)提出了广义的酸碱概念:凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+ + [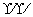 OH]- —→ H
OH]- —→ H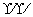 OH
OH
试指出下列两个反应中的酸或碱:
H3BO3+H2O===H++[B(OH)4]-
该反应中的碱是________(填“H3BO3”或“H2O”);
CuCl2+4NH3===[Cu(NH3)4]2++2Cl-
该反应中的酸是________(填“CuCl2”或“NH3”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
M g、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.4 8 L。下列推断中不正确的是( )
A.参加反应的Mg、Al共0.2 mo1
B.参加反应的HC1为0.4.mol
C.Mg、Al在反应中共失去0.4 mo l电子
D.若与足量的稀硫酸反应能产生0.2mo l H2
查看答案和解析>>
科目:高中化学 来源: 题型:
化工生产中常利用硫酸厂煅烧黄铁矿石的烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)来制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4·7H2O),过程如下:
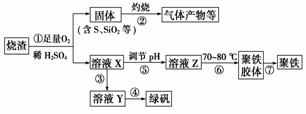
(1)将过程②中产生的气体通入下列溶液中,溶液会褪色的是________(填选项序号)。
a.品红溶液 b.紫色石蕊溶液
c.酸性KMnO4溶液 d.溴水
(2)过程①中,FeS和O2、H2SO4反应的离子方程式为______________________。
(3)过程③中,需加入的物质是______________;反应的化学方程式为________________________。用溶液Y制绿矾时,可取少量Y溶液于试管中,向试管内加入少量的________溶液,观察溶液是否变为________色,以验证其中是否含有Fe3+。
(4)在实验室里,完成过程④中的________(填操作名称),需要使用酒精灯、三脚架、坩埚钳等,还需要的玻璃仪器有__________。
(5)过程⑤调节pH,最好选用下列试剂中的________(填选项序号)。
a.稀硫酸 b.CaCO3
c.NaOH溶液 d.Fe2O3
(6)过程⑥中,将溶液Z加热到70~80 ℃,目的是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01 mol,下列叙述错误的是( )
A.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多
B.它们分别与足量CaCO3反应时,放出的CO2一样多
C.两种溶液的pH相同
D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)
B。CH3COOH属于弱酸,体积相同的两种溶液中,由n(Cl-)=
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示:
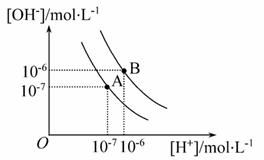
A点表示25℃时水在电离平衡时的离子浓度,当温度上升到100℃时,水的电离平衡到达B点。
(1)25℃时水的离子积为________,100℃时水的离子积为_________。
(2)100℃时,将pH=8的Ba(OH)2溶液与pH=5的稀 盐酸混合,并保持100℃恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为__________。
盐酸混合,并保持100℃恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HClO是比H2CO3还弱的酸,氯水中存在下列平衡:Cl2+H2O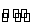 HCl
HCl
+HClO;HClO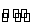 H++ClO-,达平衡后:
H++ClO-,达平衡后:
(1)要使HClO的浓度增加,可加入下列物质(填代号)________。
A.SO2 B.CaCO3 C.HCl D.NaOH
(2)由此说明在实验室里可用排饱和食盐水收集Cl2的理由是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在水溶液中1 mol Cl-、ClO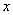 (x=1,2,3,4)的能量(kJ)相对大小如图所示。
(x=1,2,3,4)的能量(kJ)相对大小如图所示。
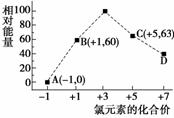
①D是________(填离子符号)。
②B—→A+C反应的热化学方程式为______________________(用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生做浓硫酸性质的实验:
在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃管口处缠放一团蘸有Na2CO3溶液的棉花。加热试管,观察现象。
回答下列问题:
(1)写出试管中发生反应的化学方程式 。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为 ,待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为 。
(3)蘸有Na2CO3溶液的棉花团作用是
。
(4)硫酸型酸雨的形成过程可用下列反应中的 来表示。
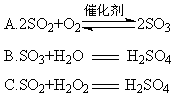
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com