
短周期元素X、Y、Z、W、R的原子序数依次增大,Y原子达到稳定结构获得的电子数目和它的内层电子数目相等,X与Z同主族,Z是所在周期主族元素中原子半径最大的元素,W的最外层电子数与电子层数相同,R与Z形成的化合物其水溶液呈碱性。下列说法正确的是
A. 离子半径由大到小的顺序为R、Z、Y、W
B. X、Y分别与Z形成的多种化合物中化学键类型相同
C. Y、R分别与X形成的化合物沸点依次升高
D. Z、W、R最高价氧化物对应的水化物两两之间均能发生反应
科目:高中化学 来源:2016-2017学年黑龙江省高二下学期开学考试化学试卷(解析版) 题型:选择题
用惰性电极电解一定浓度的CuSO4溶液时,通电一段时间后,向所得溶液中加入0.2mol Cu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解)。则电解过程中转移电子的物质的量为
A. 1.0mol B. 1.2mol C. 0.6mol D. 0.8mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(理)化学试卷(解析版) 题型:简答题
(1)刘安《淮南万毕术》中“曾青得铁则化为铜”是古代湿法炼铜的真实写照。除去CuSO4溶液中少量的Fe2+,可以按照下面的流程进行:
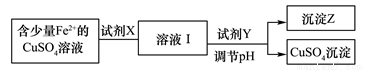
已知:Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下表:
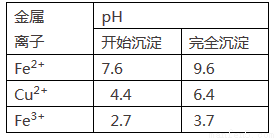
①下列物质中适合作为试剂X的是____________
A.H2O2 B.KMnO4
C.HNO3 D.Cl2
②加入的Y及调节的pH范围是_____________
A.Cu(OH)2 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
(2)已知常温下,Ksp[Cu(OH)2]=2×10-20,通过上述流程得到的CuSO4溶液中,c(Cu2+)=0.02 mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(理)化学试卷(解析版) 题型:选择题
合成氨反应:N2(g)+3H2(g) 2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是
2NH3(g) ΔH,该反应在一定条件下能自发,则下列关于该反应的ΔH、ΔS的判断,正确的是
A. ΔH<0 ΔS>0 B. ΔH<0 ΔS<0
C. ΔH>0 ΔS<0 D. ΔH>0 ΔS>0
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三适应性月考(五)理综化学试卷(解析版) 题型:填空题
甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为CO(g)+2H2(g) CH3OH(g) △H。
CH3OH(g) △H。
(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间的变化如下图甲所示。
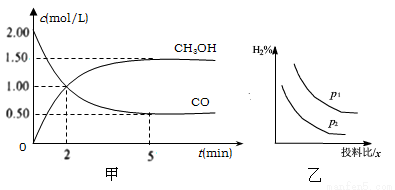
①从反应开始到5min,用氢气表示的平均反应速率v(H2)=________。
②下列说法正确的是________(填序号)。
A. 达到平衡时,H2的转化率为75%
B. 5min后容器中压强不再改变
C. 达到平衡后,再充入氩气,反应速率增大
D. 2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH2,达到平衡时容器体积为2L,且含有0.4molCH3OH(g),则该反应平衡常数的值为_______,此时向容器中再通入0.35molCO气体,则此平衡将___(填“正向移动”“不移动”或“逆向移动”)
(3)若压强、投料比x [n(CO)/n(H2)]对反应的影响如图乙所示,则图中曲线所示的压强关系:p1___p2(填“=”“>”或“<”),其判断理由是__________。
(4)甲醇是一种新型的汽车动力燃料。已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_____。
(5)现有容积均为1L的a、b、c三个密闭容器,往其中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如下图所示。b中甲醇体积分数大于a中的原因是_____。达到平衡时,a、b、c中CO的转化率大小关系为___________。
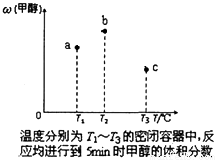
(6)甲醇作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为____。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三3月高考适应性测试理综化学试卷(解析版) 题型:简答题
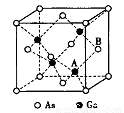
砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三3月高考适应性测试理综化学试卷(解析版) 题型:选择题
常温下,用0.10mol/LNaOH溶液滴定20.00 mL稀醋酸(HAc),下列说法中正确的是
A. 当混合溶液的pH>7时,其中不可能存在HAc分子
B. 当混合溶液的pH<7时,混合液中c(Na+)>c((Ac-)
C. 判断该滴定过程的终点,最好选择甲基橙作为指示剂
D. 达到滴定终点时,混合液中c(Na+)和c((Ac-)一定不相等
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三第二次质检化学试卷(解析版) 题型:选择题
根据如图的转化关系判断下列说法正确的是(反应条件已略去)
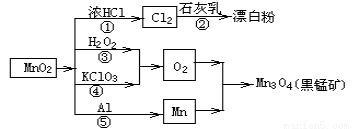
A. 反应①②③④⑤均属于氧化反应和离子反应
B. 反应⑤说明该条件下铝的还原性强于锰
C. 相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1
D. 反应①中氧化剂与还原剂的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源:2017届湖北省七市(州)高三第一次联合调考(3月联考)理科综合化学试卷(解析版) 题型:选择题
下列操作及解释都正确的是
选项 | 应用 | 解释 |
A | 在相同条件下,在两支试管中各加入2 mL 5% H2O2溶液,再向H2O2溶液中分别滴入1 mL H2O和1 mL 0.1 mol·L-1 FeCl3溶液,对比观察现象 | 可以探究催化剂FeCl3对H2O2 分解速率的影响 |
B | 向盛有1mL 0.01 mol·L-1 AgNO3溶液的试管中滴加5滴0.01 mol·L-1 NaCl溶液,有白色沉淀生成,再向其中滴加0.01 mol·L-1 KI溶液,产生黄色沉淀。 | 常温下,Ksp(AgCl)> Ksp(AgI) |
C | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出 | 蛋白质均发生变性 |
D | 保存硫酸亚铁溶液需加入少量稀盐酸和铁钉 | 防止 Fe2+水解以及被 O2 氧化 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com