
【题目】下列关于元素周期律和周期表的描述,正确的是( )
A.在元素周期表的右上方可以寻找制取半导体的元素
B.元素的性质随着原子序数的增加而呈现周期性变化
C.周期表中第ⅣA-ⅦA主族元素均可表现正化合价
D.同一主族元素的原子从上到下,原子半径减小,金属性增强
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:
【题目】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列叙述错误的是
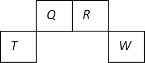
A. T的氧化物能与碱反应
B. 元素的非金属性:Q强于W
C. W的单质共热时,能与其最高价氧化物的水化物浓溶液反应
D. 原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件(温度、反应物用量等)改变,不会引起产物改变的是
A. NaOH和CO2 B. Fe粉在Cl2中燃烧
C. Na和O2 D. NaOH容液和AlCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C5H11Cl有8种同分异构体,可推知分子组成为C5H12O的醇类的同分异构体的数目是( )
A. 8种 B. 7种 C. 6种 D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:

(1)元素Ga在元素周期表中的位置为:______________。
(2)Sn的最高正价为________,Cl的最高价氧化物对应水化物的化学式为________,Bi的最高价氧化物的化学式为________。
(3)根据元素周期律,推断:
①阴影部分元素形成的氢化物中沸点最高的是________。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4________H2SeO4(填“>”、“<”、“=”或“无法比较”)。
③氢化物的还原性:H2O________H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N________Si(填“>”、“<”、“=”或“无法比较”)。
(4)可在图中分界线(虚线部分)附近寻找________(填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)若比较C、Si的非金属性强弱,请从下列试剂中选择最佳试剂组合进行实验, 请写出实验过程:(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液) _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于分散系的下列说法中,正确的是( )
A.分散系一定是混合物
B.分散剂一定是液体
C.一种分散系里只有分散质和分散剂两种物质
D.胆矾、空气、有色玻璃都是分散系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水中后有1.16g白色沉淀,在所得的悬独液中逐滴加入1mol·L-1HCl溶液,加入HCl溶液的体积V与生成沉淀的质量m的关系如图所示。试回答:
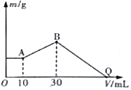
(1)A点沉淀物的化学式为_____________,
(2)AlCl3的物质的量为________________。
(3)HCl溶液在Q点的加入量是_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知干冰晶胞结构属于面心立方最密堆积,晶胞中最近的相邻两个CO2 分子间距为apm,阿伏加德罗常数为NA,下列说法正确的是
A. 晶胞中一个CO2分子的配位数是8
B. 晶胞的密度表达式是![]() g/cm3
g/cm3
C. 一个晶胞中平均含6个CO2分子
D. CO2分子的空间构型是直线形,中心C原子的杂化类型是sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com