
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铁片上发生的反应为: Fe2e===Fe2+
C. a和b用导线连接时,电子从Cu片流向铁片
D. a和b用导线连接时,Cu2+向铜电极移动
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】锌铜——稀硫酸原电池的装置如图所示,下列叙述错误的是( )

A. 电流从锌片经导线流向铜片 B. 锌是负极,其质量逐渐减小
C. 氢离子在铜表面被还原,产生气泡 D. 依据该实验现象可判断锌比铜活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是丁烷(C4H10)裂解的实验流程。连接好装置后,需进行的实验操作有:①检置整套装置的气密性②排出装置中的空气③给D、G装置加热等……;G后面装置以及铁架台等已省略;CuO能将烃氧化成CO2和H2O。

请回答下列问题:
(1)丁烷裂解的可能方程式为C4H10![]() CH4+C3H6,____________________;
CH4+C3H6,____________________;
(2)写出甲烷与氧化铜反应的化学方程式_____________________________;
(3)若对反应后E装置中的混合物(溴水足量),再按以下流程实验:
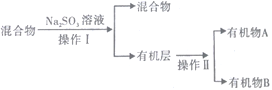
①分离操作Ⅰ和Ⅱ的名称分别是___________、___________(填字母) ;
a.蒸发 b.过滤 c.分液 d.蒸馏
②Na2SO3溶液的作用是(用离子方程式表示)_____________________________________________;
③已知A的碳原子数大于B的碳原子数,请写出B的名称______________________;
(4)假定丁烷完全裂解,流经D、G装置中的气体能完全反应。当(E+F)装置的总质量比反应前增加了0.49g,G装置的质量比反应间减少了1.44,则丁烷的裂解产物中甲烷和乙烷的物质的量之比为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通电解精炼铜的方法所制备的铜中仍含杂质,利用下面的双膜( 阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是

A. 电极a为粗铜,电极b为精铜
B. 甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
C. 乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D. 当电路中通过1mol电子时,可生成32g精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、Ag+、NO3-、Cl-B.Na+、Cu2+ 、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl-D.K+、Ba2+、CO32-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题:

(1)该反应的化学方程式为_________________。
(2)0~t1s内B气体的平均反应速率为____________。
(3)(t1+10)s时,A的转化率为_____。
(4)关于该反应的说法正确的是_________。
a.到达t1时刻该反应已停止
b.在t1时刻之前B气体的消耗速率大于它的生成速率
c.在t1时刻C气体的正反应速率等于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的熔、沸点高低顺序正确的是( )
A. 金刚石,晶体硅,二氧化硅,碳化硅 B. CI4>CBr4>CCl4>CH4
C. MgO>KCl>Hg>I2>O2 D. 金刚石>生铁>纯铁>钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味、遇水反应生成一种氯化物和两种氮化物。某学习小组在实验空用Cl2和NO制备ClNO并测定其纯度,相关实验装置(夹持装置略去)如下图所示。请回答:

(1)制备C12发生装置可以选用____(填写字母代号),请写出发生反应的离子方程式:____________。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→_______(按气流方向,用小写字母表示)。
(3)实验室可用下图装置制备亚硝酰氯(C1NO):
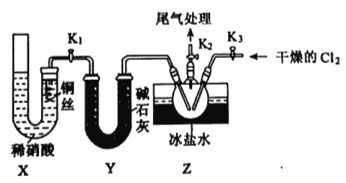
①实验室也可用B装置制备NO,X装置的优点为__________。
②检验装置气密性并装入药品,打开K2,然后再打开K1,通入一段时间气体,其目的为_______,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中C1NO可能发生反应的化学方程式为________。
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmolL-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(C1NO)的质量分数为______(用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(K2CrO4)=1×10-12]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com