
| A. | 往硫化氢水溶液中加碱有利于S2-的增加 | |
| B. | 加入催化剂有利于氨氧化的反应 | |
| C. | 高压不利于合成氨的反应 | |
| D. | 500℃左右比室温更有利于合成氨的反应 |
分析 勒夏特列原理主要内容为:在一个已经达到平衡的反应中,如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动,能用勒夏特列原理解释,首先必须存在可逆过程,以此解答该题.
解答 解:A.往H2S水溶液中加碱,碱与氢离子反应,使硫化氢的电离平衡正移,有利于S2-增多,所以能用勒夏特列原理解释,故A正确;
B、催化剂只能改变速率,不能使平衡移动,所以不能用勒夏特列原理解释,故B错误;
C、合成氨反应是体积增大的反应,增大压强,平衡正移动,能提高氨气的产量,此处高压不利于合成氨的反应,是考虑设备的耐压程度,和勒夏特列原理无关,故C错误;
D、合成氨在500℃时既可使反应速率较快,又能使催化剂的活性最好.与平衡移动原因无关,故D错误.
故选A.
点评 本题考查了勒夏特列原理的使用条件,注意使用勒夏特列原理的前提必须是可逆反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、纤维素、蔗糖、油脂都是高分子化合物 | |
| B. | 可用浓硝酸鉴别含苯环的蛋白质 | |
| C. | 工业上利用油脂在碱的催化作用下水解生产肥皂 | |
| D. | 淀粉水解与纤维素水解得到的最终产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
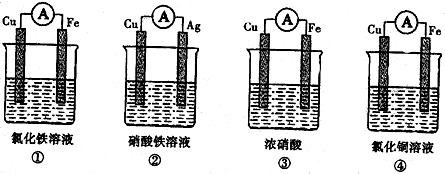
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都能发生燃烧,生成二氧化碳和水 | |
| B. | 乙炔易发生加成反应,苯只能在特殊条件下才能发生加成反应 | |
| C. | 都能被KMnO4氧化,使高锰酸钾酸性溶液褪色 | |
| D. | 相同质量的苯和乙炔,完全燃烧时耗氧量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加水稀释,盐溶液中各离子的物质的量浓度均将减小 | |
| B. | 常温下反应4Fe(OH)2+O2+2H2O═4Fe(OH)3能自发进行,则△H<0 | |
| C. | 足量的锌与等体积等pH的HA、HB溶液分别反应,HA放出的氢气少说明是强酸 | |
| D. | 反应CaSO4(s)+CO32-(aq)?CaCO3 (s)+SO42-(aq) 的实质就是沉淀溶解平衡的移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
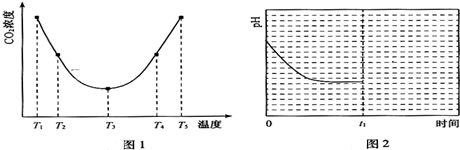
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com