
| A.金属钠投入Ca(HCO3)2溶液,反应后有白色沉淀析出 |
| B.干粉灭火器能用于扑灭金属钠、钾的着火 |
| C.生理盐水的质量分数为0.9%,与人体的血液中含量相同,它的溶质是NaCl |
| D.取用金属钠、钾时,所需实验用品有小刀、镊子、滤纸、玻璃片 |
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源:不详 题型:单选题
| A.黄色的氯化铁溶液中加入足量铁粉 |
| B.往稀硫酸中通入氨气 |
| C.往品红溶液中通入足量二氧化硫气体 |
| D.一氧化氮气体暴露在空气中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.W1>W2>W3 | B.W1=W2=W3 | C.W3>W1>W2 | D.W3>W2>W1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
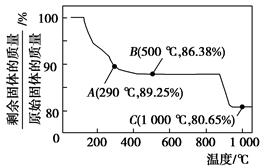
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
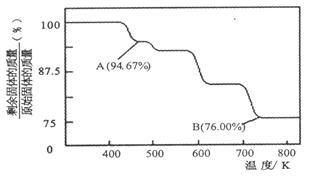
 Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。
Cr2O72-(橙色)+H2O;K=4.2×1014。若要使溶液由黄色变橙色,则应采取的措施是 。| A.加NaOH | B.加盐酸 | C.加硫酸 | D.加AgNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.复合材料一定是由两种或两种以上材料制成 |
| B.复合材料保持了原材料的优点,又有优于原材料的特点 |
| C.在复合材料中,基体起骨架作用 |
| D.在复合材料中,增强体起骨架作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上金属铈一般应低温密封保存 |
| B.工业上不能采取用H2还原氧化铈的方法冶炼金属铈 |
| C.工业上可以采用电解氯化铈水溶液米获得铈单质 |
| D.铈溶于氢碘酸的主要化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com