
(Ⅰ)水的电离平衡曲线如下图所示。

(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从 增加到 。
(2)将100℃下的pH=8的Ba(OH)2溶液与100℃下的pH=5的稀盐酸混合,并保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为 。
 (Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
(Ⅱ)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(3)若溶液中只溶解了一种溶质,该溶质的名称是 ,上述离子浓度大小顺序关系中正确的是(选填序号) 。
(4)若上述关系中C是正确的,则溶液中溶质的化学式是 。
(5)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl) c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系是c(NH4+) c(Cl-)。
(1)10-14 , 10-12 ; (2)2∶9;
(3)氯化铵 ,A (4) NH4Cl和HCl
(5) < ,=
【解析】
试题分析:(1)水的离子积Kw= c(H+)·c(OH-),根据表中数值,A点时c(H+)= c(OH-)=10-7mol/L,所以A点的 水的离子积是10-14,同理B点的水的离子积是10-6×10-6=10-12,所以从A到B点,水的离子积从10-14 增加到10-12;
(2)100℃的Kw=10-12,中性时pH=6,所以溶液pH=7,则溶液呈碱性,c(OH-)=10-5mol/L,设氢氧化钡溶液的体积是X,盐酸的体积是Y,100℃下的pH=8的Ba(OH)2溶液中c(OH-)=10-12/10-8=10-4mol/L,100℃下的pH=5的稀盐酸中c(H+)=10-5mol/L,则(10-4mol/L×X-10-5mol/L×Y)/(X+Y)= 10-5mol/L,解得X:Y=2:9;
(3)若溶液中只溶解了一种溶质,因为水电离产生氢氧根离子和氢离子,所以溶质只能是氯化铵,此时溶液呈酸性,铵根离子水解,所以氯离子浓度大于铵根离子浓度,则离子浓度的关系是c(Cl-)>c(NH4+)>c(H+)>c(OH-),答案选A;
(4)若溶液中离子浓度大小顺序为c(Cl-)>c(H+)>c(NH4+)>c(OH-),说明溶液呈酸性,且氢离子浓度大于铵根离子浓度,说明该溶液的溶质为HCl和NH4Cl,且HCl的浓度大于氯化铵的浓度;
(5)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,若二者等物质的量浓度,则反应后的溶液为氯化铵溶液,溶液呈酸性,现在溶液呈中性,则氨水的物质的量大于HCl的物质的量,所以混合前c(HCl)< c(NH3·H2O);混合后溶液呈中性,则c(OH-)=c(H+),根据电荷守恒,则c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以c(Cl-)=c(NH4+)。
考点:考查水的离子积的计算与应用,溶液中离子浓度的比较


科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
实验室用0.10mol/L的NaOH溶液滴定某一元弱酸HA的滴定曲线如图所示。图中横轴为滴入的NaOH溶液的体积V(mL),纵轴为溶液的pH。下列叙述不正确的是

A.此一元弱酸HA的电离平衡常数Ka≈1×10-6mol/L
B.此弱酸的起始浓度约为1×10-2mol/L
C.此实验最好选用酚酞试液(变色范围8.0~10.0)做指示剂
D.当混合液pH=7时,溶液中c(HA)>c(A—)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
(12分)【化学——物质结构与性质】铜及其化合物是重要的化工原料。请回答下列问题:
(1)与铜同周期的所有元素的基态原子中,未成对电子数与铜原子相同的元素有 种。Cu+的电子排布式是 。
(2)配离子[Cu(NH3)4(H2O)2]2+含有的微粒间的作用力类型有 ;H、N、O三种元素的第一电离能由大到小的顺序是 。
(3)EDTA( )也可以与铜离子形成配合物。其中碳原子轨道的杂化类型为 。
)也可以与铜离子形成配合物。其中碳原子轨道的杂化类型为 。
(4)CuCl的晶胞结构如图所示,

其中C1-的配位数(即与C1-最近距离的Cu+的个数)为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.1mol莽草酸与足量金属Na反应生成生成0.5mol H2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
如图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是

①Fe;②HNO3;③Na;④C
A.①②③ B.②③④ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是
A、将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨Mg的活泼性
B、将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成
C、将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀
D、将Mg(OH)2沉淀转入表面皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:填空题
(8分)常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L HCl溶液和
20.00 mL 0.1000 mol/L CH3COOH溶液,得到2条滴定曲线,如下图所示:
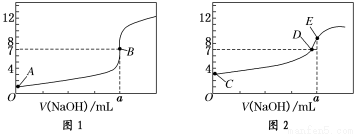
(1)由A、C点判断,滴定HCl溶液的曲线是______(填“图1”或“图2”);
(2)a=________ mL;
(3)c(Na+)=c(CH3COO-)的点是________;
(4)E点对应离子浓度由大到小的顺序为________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列生产生活中常见物质的主要成分与化学式相对应的是
A.光导纤维—Si B.铝土矿—Al(OH)3
C.水泥—Na2SiO3 D.明矾—KAl(SO4)2·12H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com