
【题目】某课外活动小组欲利用氨气与CuO反应,研究氨气的性质并测其组成,设计了如下实验(夹持装置未画出)进行实验。请回答下列问题:

(1)仪器a的名称为____________;仪器b中可选择的试剂为(任意填一种)_____________。
(2)实验中,装置C中黑色CuO粉末全部转化为红色固体(已知Cu2O也为红色固体),量气管中有无色无味的气体。实验前称取黑色CuO 80g,实验后得到红色固体质量为68g。则红色固体成分的化学式为_______________。
(3)E装置中浓硫酸的作用是____________________________________。
(4)F中读取气体体积前,应对装置F进行的操作是:___________________,若无此操作,而F中左边液面低于右边液面,会导致读取的气体体积________ (填“偏大”或“偏小”或“无影响”);图中量气管可由________ (请选择字母填空:A.酸式滴定管,B.碱式滴定管)改装而成。
(5)要想测得氨气分子中氮、氢原子个数比,实验中应至少测量或读取哪些数据________。
A.B装置实验前后质量差mg; B.F装置实验前后液面差VL
C.D装置实验前后质量差mg; D.E装置实验前后质量差mg;
【答案】(1)分液漏斗(1分) 碱石灰或生石灰或氢氧化钠固体(任意填一种)(2分)
(2)Cu和Cu2O(3分)
(3)防止F中水蒸气进入D中,并吸收氨气(2分)
(4)向上或向下移动右管,使得左右两边液面相平(2分),偏小(2分),B(1分)
(5)B、C(2分)
【解析】
试题(1)a是分液漏斗,A是制氨气的装置,所以b中可放碱石灰或生石灰或氢氧化钠固体任意一种
(2)若CuO全部被还原为Cu,则CuO∽Cu,计算出Cu的质量为64g,但红色固体的质量为68g>64g,所以该红色固体的成分是Cu和Cu2O
(3)浓硫酸的作用是吸收未反应的氨气及防止F中的水进入D中,影响结果
(4)F中读取气体体积时应保证气体和外界大气压相等,所以应向上或向下移动右管,使得左右两边液面相平,若F中左边液面低于右边液面,说明气体压强大于外界大气压强,压强增大体积偏小,根据酸式滴定管与碱式滴定管的不同,图中量器管可由碱式滴定管改装而成,选B
(5)确定氨气分子中氮、氢原子个数比也即确定产物中水和氮气的物质的量,A、B装置是干燥氨气,其质量与所求无关,错误;B、F装置测量氮气的体积,正确;C、D装置测量产物水的质量,正确;D、E装置是吸收多余的氨气及防治水进入D中,与所求无关,所以答案选B、C


科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)===2SO3(g)反应过程的能量变化如图所示。
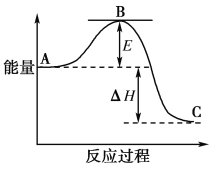
已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示______________、________________,E的大小对该反应的反应热________(填“有”或“无”)影响;
(2)该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________________________________________________________________________________;
(3)图中ΔH=________kJ·mol-1;
(4)已知单质硫的燃烧热ΔH=-296 kJ·mol-1,计算由S(s)生成1 mol SO3(g)的ΔH________(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中互为同系物的是( )
A. CH3—CH2—CH3和CH3—CH2—CH2—CH2—CH3B. CH3—CH3和CH3—CH![]() CH2
CH2
C. CH3—CH2—CH3和CH3—CH![]() CH2D. CH3—CH2—CH
CH2D. CH3—CH2—CH![]() CH2 和CH3—CH2—CH2—CH3
CH2 和CH3—CH2—CH2—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D的原子序数依次增大,B和D同主族;X、Y、N分别是由以上四种元素中两种组成的化合物,Z是由以上三种元素组成的化合物;若X与Y的摩尔质量相同,Y为淡黄色固体,N常温下是液体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )

A. 相对分子质量M>N,沸点M>N
B. 原子半径:D>B>C>A
C. Z 为 NaOH
D. M中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、T、U五种短周期元素。X、Y、Z 三元素在周期表中的位置如图所示,三元素的原子序数之和是 41。X 和 T 的单质在不同条件下反应,可以生成T2X(白色固体)和T2X2(淡黄色固体)两种化合物。U 单质在 Z 单质中燃烧时产生苍白色火焰,生成物的水溶液能使石蕊试液变红。
X | |
Y | Z |
(1)各元素的符号是 X______,Y______,Z______。
(2)Y 原子的结构示意图为_______。
(3)用电子式表示 Y 与 T 组成的化合物的形成过程:______。
(4)YX2 和 U2Y 反应的化学方程式为______, 其中氧化剂是______,被氧化的元素是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如右:

回答下列问题:
(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为:__________________、_______________。
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是___________,滤渣是________;过滤操作②的滤液是____________和____________,滤渣是_______。
(3)工艺过程中③和④的目的是______________。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是____________________。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。
称量草酸成品0.250 g溶于水,用0.0500 mol·L-1的酸性KMnO4溶液滴定,至浅粉红色不消褪,消耗KMnO4溶液15.00 mL,反应的离子方程式为__________________;
列式计算该成品的纯度____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化铝是一种重要的化工原料,工业上利用明矾石制备无水氯化铝的流程如下,请回答下列问题:

(1) 实验室中,可制得Cl2的组合是____________(填代号)。
①MnO2和浓盐酸混合共热 ②MnO2、NaCl和浓硫酸混合共热
③NaClO和盐酸混合共热 ④漂白粉和硫酸混合共热
(2) 吸收焙烧炉中产生的尾气,下列装置合理的是___________(填代号)。

(3)写出氧化炉中反应的化学方程式_____________。
(4)生产氯化铝的过程中焙烧炉和氯化炉中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少污染。试设计简单实验检验二者是否恰好完全反应,简要描述实验步骤、现象和结论_____________(仪器自选)。
可供选择试剂如下:
①滴加酚酞的氢氧化钠溶液 ②氣化亚铁溶液 ③硫氰化钾溶液 ④品红溶液
(5)某同学设计用如下装置验证二氧化硫的某些化学性质。

① 能说明二氧化硫具有氧化性的实验现象为____________。
② 写出a瓶中发生反应的离子方程式________________。
③ 充分反应后,取a瓶中的溶液分成三份,分别进行如下实验。
实验I:向第一份溶液中加入足量的NaOH溶液,生成白色沉淀,迅速变为灰绿色,最终变为红褐色。
实验II:向第二份溶液中加入少量KMnO4溶液,紫色褪去。
实验III:向第三份溶液中加人BaCl2溶液,生成白色沉淀。
上述实验中能充分证明二氧化硫具有还原性的是__________(填实验代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC﹣COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为________;
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有______(填“氧化性”、“还原性”或“酸性”);②请配平该反应的离子方程式:_____MnO4-+____H2C2O4+___H+=___Mn2++____CO2↑+_____H2O
(3)将一定量的乙二酸放于试管中,按如图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红。据此回答:
①上述装置中,D的作用是_________,
②乙二酸分解的化学方程式为 ________;
(4)该小组同学将2.52g草酸晶体(H2C2O42H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是_______(用文字简单表述),该溶液中各离子的浓度由大到小的顺序为:_______(用离子符号表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,
时,![]() 及其钠盐的溶液中,H2SO3、HSO3-、SO32-的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
及其钠盐的溶液中,H2SO3、HSO3-、SO32-的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )

A. 溶液的pH=5时,硫元素的主要存在形式为![]()
B. 当溶液恰好呈中性时: c(Na+)>c(HSO3-)+c(SO32-)
C. 向pH=8的上述溶液中滴加少量澄清石灰水, 的值增大
的值增大
D. 向pH=3的上述溶液中滴加少量稀硫酸,![]() 减小
减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com