
| A. | ①② | B. | ③④ | C. | ③④⑤ | D. | ⑤⑥ |
分析 ①二氧化硅和氢氧化钠溶液反应生成硅酸钠和水;
②Fe(OH)2与氧气、水反应生成Fe(OH)3;
③二氧化硅不能溶于水得到硅酸;
④氧化铝不能一步反应得到氢氧化铝;
⑤过氧化钠和盐酸反应生成氯化钠、水和氧气;
⑥偏氯酸钠与过量盐酸反应生成氯化铝.
解答 解:①二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,SiO2+2NaOH=Na2SiO3+H2O,一步反应实现,故①不选;
②Fe(OH)2→Fe(OH)3,氢氧化亚铁能与空气和水反应生成氢氧化铁,能一步实现,故②不选;
③二氧化硅不能溶于水得到硅酸,一步反应不能实现,故③选;
④氧化铝不能一步反应得到氢氧化铝,一步反应不能实现,故④选;
⑤过氧化钠和盐酸反应生成氯化钠、水和氧气,2Na2O2+4HCl=4NaCl+2H2O+O2↑,一步反应实现,故⑤不选;
⑥偏氯酸钠与过量盐酸反应生成氯化铝,可一步实现,故⑥不选;
故选B.
点评 本题考查物质之间转化,多角度考查元素化合物知识,明确物质的性质是解本题关键,熟记元素化合物知识,知道硅酸的制取方法,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 联合制碱法中循环使用CO2和NH3,以提高原料利用率 | |
| B. | 硫酸工业中,SO2氧化为SO3时采用常压,因为高压会降低SO2转化率 | |
| C. | 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |
| D. | 炼钢是在高温下利用氧化剂把生铁中过多的碳和其他杂质氧化成气体或炉渣除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磷在氯气中燃烧产生大量的白烟,并放出热量 | |
| B. | 纯净的氢气在氯气中安静燃烧,发出黄色火焰 | |
| C. | 光照新制氯水有气泡逸出,该气体是Cl2 | |
| D. | 实验室制备氯气可用排饱和食盐水法收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠是一种灰黑色、具有金属光泽、质地软的金属 | |
| B. | 氧化钠与过氧化钠的颜色不同 | |
| C. | 因为钠的性质非常活泼,故自然界中无游离态钠 | |
| D. | 过氧化钠可以做潜艇的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
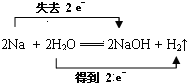 反应中,H2O是氧化剂.
反应中,H2O是氧化剂.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com