
下列实验操作、现象和解释都正确的是(双选)( )
| 选项 | 实验操作 | 现象 | 解释 |
| A. | 向某溶液中加入盐酸 | 产生无色气体 | 溶液中一定含有CO |
| B. | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
| C. | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 上层呈紫红色,下层有白色沉淀生成 | 铜离子可以氧化碘离子,白色沉淀可能成为CuI |
| D. | 向某无色溶液中滴加硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 溶液中一定含有SO |
科目:高中化学 来源: 题型:
把0.02 mol·L-1 CH3COOH溶液和0.01 mol·L-1 NaOH溶液以等体积混合,溶液呈酸性,混合溶液中粒子浓度关系正确的是( )
A.[CH3COO-]>[Na+]
B.[CH3COOH]>[CH3COO-]
C.2[H+]=[CH3COO-]-[CH3COOH]
D.[CH3COOH]+[CH3COO-]=0.02 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
2NO(g) +O2(g)2NO2(g) 。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
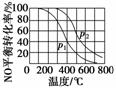
①比较p1、p2的大小关系________。
②随温度升高,该反应平衡常数变化的趋势是________。
(2)[2014·广东理综,31(2)(3)(4)]用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
① 1/4CaSO4(s)+CO(g)1/4CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
② CaSO4(s)+CO(g)CaO(s)+CO2(g) +SO2(g) ΔH2=+210.5 kJ·mol-1
③ CO(g)1/2C(s)+1/2CO2(g) ΔH3=-86.2 kJ·mol-1
①反应①~③的平衡常数的对数lgK随反应温度T的变化曲线见下图,结合各反应的ΔH,归纳lgK~T曲线变化规律:

a.__________________________________________________________;
b.__________________________________________________________。
②向盛有CaSO4的真空恒容密闭容器中充入CO,反应①于900 ℃达到平衡,c平衡(CO)=8.0×10-5 mol·L-1,计算CO的转化率(忽略副反应,结果保留两位有效数字)。
③为减少副产物,获得更纯净的CO2,可在初始燃料中适量加入________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:

(1)气体A中的大气污染物可选用下列试剂中的_________吸收。
a.浓硫酸 b.稀硝酸
c.NaOH溶液 d.氨水
(2)用稀硫酸浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_______(填离子符号),检验溶液中还存在Fe2+的方法是____________(注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学方程式为_________________________________。
(4)以CuSO4溶液 为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的
为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的 是__________。
是__________。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(5)利用反应2Cu+O2+2H2SO4====2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的铁粉中加入稀硝酸,充分反应后,滴入KSCN溶液 | 溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀的KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 铝箔插入稀硝酸中 | 无现象 | 铝箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验装置图正确的是(双选)( )。
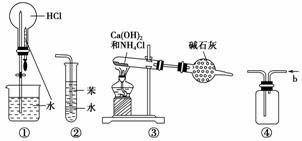
A.装置①可用于做HCl喷泉实验
B.装置②可用于吸收HCl气体,并防倒吸
C.装置③可用于实验室制备少量NH3
D.装置④b口进气可收集CO2等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.向蔗糖水解后的溶液中直接加入少量银氨溶液,可证明生成了葡萄糖
B.淀粉与纤维素、葡萄糖与果糖均互为同分异构体
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液pH>7,原因是__________________(用离子反应方程式表示)。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是____________。
(3)在1 mol·L-1的KAl(SO4)2溶液中离子浓度由大到小的顺序是____________。
(4)某小组同学用下图所示装置探究NaClO和KAl(SO4)2饱和溶液混合反应的实验。
①打开活塞向烧瓶中加入饱和KAl(SO 4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是_____________________________________________________。
4)2溶液,产生大量的白色胶状沉淀。反应的离子方程式是_____________________________________________________。
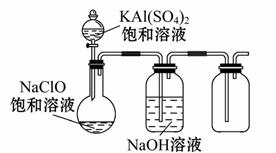
②将烧瓶中的混合液在阳光下照射,不久烧瓶中有黄绿色气体产生。充分反应后集气瓶中气体能使带火星的木条复燃。写出在光照下混合液中反应的化学方程式______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com