
A.水分子的结构式为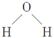 |
| B.氧与氟形成的化合物(OF2)中,氧元素的化合价为-2价 |
| C.Na2O2的电子式为Na+[··············]2-Na+ |
D.在MgO晶体中,O2-的结构示意图可表示为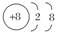 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:不详 题型:单选题
| A.NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8电子稳定结构; |
| B.P4和CH4都是正四面体分子且键角都为109o28ˊ; |
| C.NaCl晶体中与每个Na+距离相等且最近的Na+共有12个; |
| D.单质的晶体中一定不存在的微粒是阳离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.S2Cl2分子中各原子均达到8电子稳定结构 |
| B.S2Cl2结构中的化学键只含有极性键 |
| C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 |
| D.S2Cl2与H2O反应的生成物中可能有S |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分子中3个原子的最外层电子数之和可能为21 |
| B.该分子的空间构型可能为折线型 |
| C.该分子可能是极性分子,也可能是非极性分子 |
| D.该分子中3个原子一定共平面 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
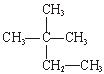 ③白磷 ④氯气 ⑤
③白磷 ④氯气 ⑤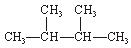
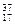 Cl ⑦
Cl ⑦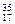 Cl ⑧红磷
Cl ⑧红磷查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
 较,NH3 HF(选填“>”或“<”);
较,NH3 HF(选填“>”或“<”);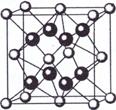
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.HCl、HBr、HI的熔、沸点最低的是 HCl |
| B.磷原子核外有15个运动状态完全不同的电子 |
| C.硝酸易挥发是因为形成分子内氢键 |
| D.甲烷分子间也可以形成氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com