
 ×100% ②C=
×100% ②C= ③上述溶液中再加入VmL水后,所得溶液的质量分数大
③上述溶液中再加入VmL水后,所得溶液的质量分数大| A.②④ | B.②③ | C.①③ | D.①④ |
科目:高中化学 来源:不详 题型:单选题
| A.18gH218O分子中含有的10NA个质子 |
| B.将3mol NO2完全溶于水,生成NO气体,气体的物质的量变为2mol |
| C.将1.5molCO2气体通入到1L 1mol/L的NaOH溶液中,生成1mol碳酸钠 |
| D.2Cu2S+2H2SO4+5O2=4CuSO4+2H2O反应中,当1mol O2发生反应时,还原剂所失电子的物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
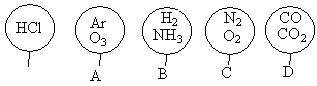
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.③④ | C.①③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.150 mL 1 mol·L-1的NaCl | B.25 mL 2 mol·L-1的FeCl3 |
| C.150 mL 3 mol·L-1的KCl | D.75 mL 2 mol·L-1的CaCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.012 kg12C含有6.02×1023个碳原子 | B.1mol任何物质都含有6.02×1023个原子 |
| C.硫酸的摩尔质量是98g | D.常温常压下,1 mol氧气的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.7.84L | B.6.72L | C.4.48L | D.无法计算 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com