

·ÖĪö ³£¼ūĖ«Ō×Óµ„ÖŹ·Ö×ÓÖŠ£¬ŗ¬¹²¼Ū¼üŹżÄæ×ī¶ąµÄŹĒN2£¬¼“XĪŖN2£¬·Ö×ÓÖŠŗ¬ÓŠ3øö¹²¼Ū¼ü£¬µ„ÖŹX”¢Y”¢ZŌŚĶس£×“æöĻĀ¾łĪŖĘųĢ¬£¬Ó¦ĪŖ·Ē½šŹō£¬·Ö±š·“Ӧɜ³É»ÆŗĻĪļ¼×”¢ŅŅ£¬¶žÕß·“Ӧɜ³ÉĄė×Ó»ÆŗĻĪļ£¬Ó¦ĪŖļ§ŃĪ£¬Ōņ»ÆŗĻĪļ¼×ĪŖNH3£¬YĪŖH2£¬ŅŅĪŖĒā»ÆĪļ£¬ÄÜÓė°±Ęų·“Ӧɜ³ÉŃĪ£¬ĒŅŗ¬ÓŠ18øöµē×Ó£¬Ó¦ĪŖHCl£¬ŌņZĪŖCl2£¬±ūĪŖNH4Cl£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ¼ūĖ«Ō×Óµ„ÖŹ·Ö×ÓÖŠ£¬ŗ¬¹²¼Ū¼üŹżÄæ×ī¶ąµÄŹĒN2£¬¼“XĪŖN2£¬·Ö×ÓÖŠŗ¬ÓŠ3øö¹²¼Ū¼ü£¬µ„ÖŹX”¢Y”¢ZŌŚĶس£×“æöĻĀ¾łĪŖĘųĢ¬£¬Ó¦ĪŖ·Ē½šŹō£¬·Ö±š·“Ӧɜ³É»ÆŗĻĪļ¼×”¢ŅŅ£¬¶žÕß·“Ӧɜ³ÉĄė×Ó»ÆŗĻĪļ£¬Ó¦ĪŖļ§ŃĪ£¬Ōņ»ÆŗĻĪļ¼×ĪŖNH3£¬YĪŖH2£¬ŅŅĪŖĒā»ÆĪļ£¬ÄÜÓė°±Ęų·“Ӧɜ³ÉŃĪ£¬ĒŅŗ¬ÓŠ18øöµē×Ó£¬Ó¦ĪŖHCl£¬ŌņZĪŖCl2£¬±ūĪŖNH4Cl£¬
£Ø1£©ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬»ÆŗĻĪļ±ūÖŠŃōĄė×ÓÕāļ§øłĄė×Ó£¬¼ģŃéļ§øłĄė×ӵķ½·ØŹĒŌŚŃłĘ·ČÜŅŗÖŠµĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬¼ÓČČ£¬ÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃ飬ČōÓŠÄÜŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢå²śÉś£¬Ōņѳʷ֊ŗ¬ÓŠļ§øłĄė×Ó£¬·ńŌņƻӊļ§øłĄė×Ó£¬
¹Ź“š°øĪŖ£ŗŌŚŃłĘ·ČÜŅŗÖŠµĪ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬¼ÓČČ£¬ÓĆŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½¼ģŃ飬ČōÓŠÄÜŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢå²śÉś£¬Ōņѳʷ֊ŗ¬ÓŠļ§øłĄė×Ó£¬·ńŌņƻӊļ§øłĄė×Ó£»
£Ø2£©¢ŁŹŌ¹ÜÖŠŹĒÖʱø°±ĘųµÄ·“Ó¦£¬ĖłŃ”µÄŹŌ¼ĮŹĒNH4ClŗĶCa£ØOH£©2£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ2NH4Cl+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗ2NH4Cl+Ca£ØOH£©2$\frac{\underline{\;\;”÷\;\;}}{\;}$CaCl2+2NH3”ü+2H2O£»
¢Ś°±Ęų¼«Ņ×ČÜÓŚĖ®£¬ÉÕ±ÖŠŠĪ³ÉŅ»Ė®ŗĻ°±ČÜŅŗ£¬Ņ»Ė®ŗĻ°±“ęŌŚµēĄėÉś³Éļ§øłĄė×ÓŗĶĒāŃõøłĄė×Ó£¬¼“NH3•H2O?NH4++OH-£¬ĻŌ¼īŠŌ£¬Óöµ½·ÓĢŖÓÉĪŽÉ«±äĪŖŗģÉ«£¬
¹Ź“š°øĪŖ£ŗNH3•H2O?NH4++OH-£»
¢ŪŹµŃéÖŠ½«°±Ė®µÄÅØČÜŅŗµĪ¼ÓÖĮ¼īŹÆ»Ņ»ņŃõ»ÆøĘÖŠæÉæģĖŁÖʱø°±Ęų£¬¹ŹŃ”bc£»
£Ø3£©XĪŖN2£¬YĪŖH2£¬X”¢YÖŠµÄŌŖĖŲæÉ×é³É¾ßÓŠ18øöµē×ӵķÖ×ÓĪŖN2H4£¬¹Ź“š°øĪŖ£ŗN2H4£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹŠŌÖŹµÄ·ÖĪöÅŠ¶Ļ£¬×Ŗ»Æ¹ŲĻµŗĶĪļÖŹŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬ÕĘĪÕĪļÖŹŠŌÖŹŗĶĢŲÕ÷·“Ó¦²śĪļµÄ·ÖĪöÅŠ¶Ļ£¬ŹµŃéÖʱøĘųĢåµÄ×°ÖĆŃ”ŌńŗĶŠŌÖŹŃéÖ¤£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
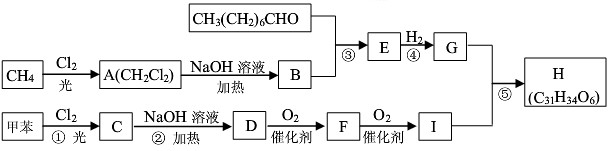
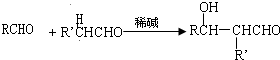
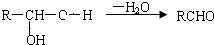
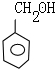 £¬E
£¬E £®
£® £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X”¢MĮ½ÖÖŌŖĖŲÖ»ÄÜŠĪ³ÉX2MŠĶ»ÆŗĻĪļ | |
| B£® | ÓÉY”¢MĮ½ÖÖŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļŹĒĄė×Ó»ÆŗĻĪļ | |
| C£® | MµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČZµÄČõ | |
| D£® | Ō×Ó°ė¾¶£ŗr£ØM£©£¼r£ØW£©£¾r£ØZ£©£¼r£ØY£©£¼r£ØX£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬11.2LCCl4ÖŠŗ¬ÓŠµÄ·Ö×ÓŹżÄæĪŖ0.5NA | |
| B£® | ³£ĪĀĻĀ£¬1L0.1mol/LCH3COOHČÜŅŗÖŠŗ¬ÓŠµÄH+ŹżÄæĪŖ0.1NA | |
| C£® | 25”ę£¬PH=13µÄNaOHČÜŅŗÖŠŗ¬ÓŠOH-µÄŹżÄæĪŖ0.1NA | |
| D£® | 1L 1mol/LµÄNH4ClČÜŅŗÖŠ£¬Ėłŗ¬NH4+µÄŹżÄæŠ”ÓŚNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ĻņAlCl3ČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ£¬ČēĶ¼£¬ĒśĻߢŁ”¢¢Ś·Ö±š±ķŹ¾Į½ÖÖĪļÖŹµÄĪļÖŹµÄĮæµÄ±ä»Æ£®ĘäÖŠÕżČ·µÄŹĒ£Ø””””£©
ĻņAlCl3ČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ£¬ČēĶ¼£¬ĒśĻߢŁ”¢¢Ś·Ö±š±ķŹ¾Į½ÖÖĪļÖŹµÄĪļÖŹµÄĮæµÄ±ä»Æ£®ĘäÖŠÕżČ·µÄŹĒ£Ø””””£©| A£® | ¢ŁAl3+ ¢ŚAl£ØOH£©3 | B£® | ¢ŁAl3+ ¢ŚAlO2- | ||
| C£® | ¢ŁAl£ØOH£©3 ¢ŚAl3+ | D£® | ¢ŁAlO2- ¢ŚAl3+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1øöĒāĘų·Ö×ӵďµ¼ŹÖŹĮæŌ¼ĪŖ£Ø1/NA £©g | |
| B£® | ŗ¬NAøöŃõŌ×ÓµÄŃõĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ22.4 L | |
| C£® | ¹żŃõ»ÆÄĘÓėĖ®·“Ó¦£¬Ćæ²śÉś±ź×¼×“æöĻĀ11.2 L O2£¬×ŖŅĘNAøöµē×Ó | |
| D£® | 1 mol Na Ō×ÓÖŠŌ¼ŗ¬ÓŠNAøöµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ā±“śĢž²»ŹĒĢž | B£® | ŗ¬ōĒ»łµÄ»ÆŗĻĪļŅ»¶ØŹĒ“¼ | ||
| C£® | ·¼ĻćĢž²»ŹĒĢž | D£® | ŗ¬Č©»łµÄ»ÆŗĻĪļŅ»¶ØŹĒČ© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com