
下列物质,所含分子数最多的是(NA表示阿伏加德罗常数的值)
A.10g H2 B.2mol Cl2
C.1.5NA CO2 D.22.4L O2(标况下)
科目:高中化学 来源:2015-2016学年江苏省高二上学期期中必修化学试卷(解析版) 题型:选择题
有200mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为
A.65mL B.72mL C.80mL D.128mL
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期第二次月考化学试卷(解析版) 题型:选择题
某无色溶液,溶质仅由Na+、Ag+、Ba2+、Al3+、AlO2─、MnO4─、CO32─、SO42─中的若干种组成。取该溶液进行如下实验:
⑴ 取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液;
⑵ 在⑴所得溶液中加入过量NH4HCO3溶液,有气体生成,同时析出白色沉淀甲;
⑶ 在⑵所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时析出白色沉淀乙。
则下列离子在原溶液中一定存在的有
A、SO42-、AlO2─、Na+、CO32─ B、Na+、CO32─、AlO2─
C、CO32─、Na+、Al3+ D、MnO4─、Na+、CO32─
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江大庆实验中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A、用广泛pH试纸测氯水的pH=4
B、欲配制1L,1mol/L的NaCl溶液,可将58.5gNaCl溶于1 L水中
C、配制溶液定容时,仰视容量瓶刻度会使所配溶液浓度偏低
D、用瓷坩埚加热熔化氢氧化钠固体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NACl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定实验时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源:2016届山西怀仁第一中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.电解氯化镁溶液: 2Cl- + 2H2O===== Cl2 ↑+ H2↑+ 2OH-
B.向AlCl3溶液中加入过量的氨水: Al3+ + 4NH3·H2O=====AlO2-+ 4NH4++ 2H2O
C.Cu与浓硝酸反应制备NO2: 3Cu + 8H+ + 2NO3-=====3Cu2+ + 2NO2↑ + 4H2O
D.向KAl(S04)2溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:Al3+ + 2SO42- + 2Ba2+ + 4OH-=====AlO2-+ 2BaSO4 ↓+ 2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016河北石家庄第一中学高一上期中考试化学试卷(解析版) 题型:选择题
一定条件下,当溶液中XO4-与H2O2分子个数比恰好为2︰5时,溶液中XO4-离子被还原为较低价态,则X元素的化合价变为
A.+2 B.+3 C.+4 D.+5
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:填空题
决定物质性质的重要因素是物质的结构。请回答下列问题:
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显 价,A的电负性 B的电负性(填“>”、“<”或“=”)。
(2)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似。下表是3种离子晶体的晶格能数据:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3401 |
离子键的强弱可以用离子晶体的晶格能来衡量,KCl、CaO、TiN 3种离子晶体熔点从高到低的顺序是 。MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
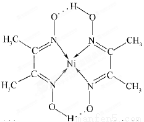
(4)某配合物的分子结构如图所示,其分子内不含有 (填字母)。
A.离子键 B.共价键 C.配位键 D.氢键
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高级中学高三第四次模拟考试理化学卷(解析版) 题型:填空题
研究N0x、SO2等大气污染气体的处理有重要意义。
(1)NO2可用水吸收,相应的化学方程式为 。利用反应:6NO2+8NH3 7N2+12H2O也可以处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_________L。
7N2+12H2O也可以处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是_________L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1;
2SO3(g) ΔH=-196.6 kJ·mol-1;
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol-1;
2NO2(g) ΔH=-113.0 kJ·mol-1;
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=_________ kJ·mol-1。(3)大气中SO2和NOx是形成酸雨的主要污染气体。某地酸雨中可能含有下列离子:Na+、Mg2+、NH4+、Cl-、SO32-、SO42-、NO3-和NO2-等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。已知:Ksp(Ag2SO4)=1.20×10-5
SO3(g)+NO(g)的ΔH=_________ kJ·mol-1。(3)大气中SO2和NOx是形成酸雨的主要污染气体。某地酸雨中可能含有下列离子:Na+、Mg2+、NH4+、Cl-、SO32-、SO42-、NO3-和NO2-等。某研究小组取该地一定量的酸雨,浓缩后将所得试液分成4份,进行如下实验:第一份酸化后滴加适量的淀粉KI溶液,呈蓝色;第二份滴加用盐酸酸化的BaCl2溶液,有白色沉淀析出;第三份滴加NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝;第四份加入硝酸酸化的AgNO3溶液,有沉淀产生,静置,在上层清液中滴加酸性KMnO4溶液,不褪色。已知:Ksp(Ag2SO4)=1.20×10-5
请回答下列问题:
①该酸雨中肯定存在的离子有_______;肯定不存在的离子有______,说明其不存在的理由:_____。
②写出试液中滴加淀粉KI溶液所发生反应的离子方程式:____________。
③该研究小组为了探究NO参与的硫酸型酸雨的形成,在烧瓶中充入含有少量NO的SO2气体,慢慢通入O2,该过程中发生的化学反应有2NO+O2=2NO2 、 NO2+SO2=SO3 + NO,再喷射适量蒸馏水即得硫酸型酸雨。说明NO的作用:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com