
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.X、Y的简单离子半径:r(X2﹣)>r(Y+)
B.Y2X和Y2X2中阴、阳离子的个数比相同,化学键类型也完全相同
C.M与X形成的化合物对应的水化物一定是强酸
D.M的气态氢化物比N的气态氢化物稳定
科目:高中化学 来源:2015-2016学年安徽师大附属中学高二上期中测试化学试卷(解析版) 题型:选择题
有人设想合成具有以下结构的烃分子,下列说法不正确的是

A.Ⅳ不可能合成得到
B.Ⅱ与苯互为同分异构体
C.Ⅲ(立方烷)的六氯代物共有3种
D.Ⅰ中各键之间夹角为109°28’
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列关于物质分类的说法正确的是
A.根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸
B.根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
C.铝热剂、福尔马林、水玻璃、漂白粉均为混合物
D.明矾、水银、烧碱、硫酸均为强电解质
查看答案和解析>>
科目:高中化学 来源:2016届西藏拉萨中学高三上学期第二次月考化学试卷(解析版) 题型:填空题
(15 分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,根据要求解决下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为 (3分)。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
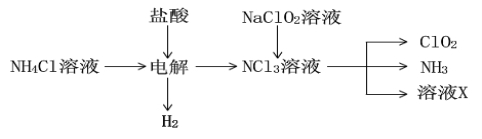
①电解时发生反应的化学方程式为 (3分)。
②溶液X中大量存在的阴离子有__________________。
③除去ClO2中的NH3可选用的试剂是 (填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(3)为了测定混合气体中ClO2的含量,我们通常用酸化的KI溶液与之反应。
①请写出ClO2与碘化钾反应的离子方程式为 (3分)。
②如果反应过程中共消耗了 0.04 mol的KI,则此混合气体中ClO2的质量为________克。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春市高三上学期质量监测化学试卷(解析版) 题型:填空题
[化学—选修(二)化学与技术](15分)常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害。某化学兴趣小组拟采用如下处理方法回收废电池中的各种资源。
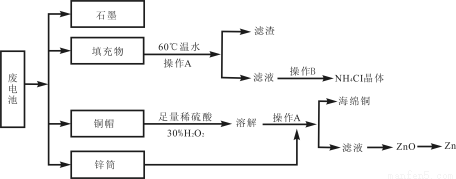
(1)填充物用60℃温水溶解,目的是 。
(2)操作A的名称为 。
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示)。铜帽溶解完全后,可采用_________方法除去溶液中过量的H2O2。
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 。
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止。主要反应为 2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O。
①当1 mol MnO2参加反应时,共有 mol电子发生转移。
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该应的化学方程式: 。
(6)锌锰干电池所含的汞可用KMnO4溶液吸收。在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如下图所示:
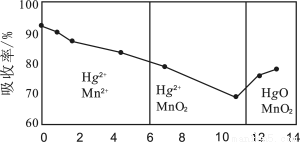
根据上图可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率 。
②在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下 强。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春市高三上学期质量监测化学试卷(解析版) 题型:选择题
下列解释实验事实的离子方程式正确的是
A.用氢氧化钠溶液吸收氯气:Cl2+2OH﹣═ ClO﹣+Cl﹣+H2O
B.用大理石与稀盐酸制备二氧化碳:CO32﹣+2H+═ CO2↑+H2O
C.稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2++SO42﹣═ BaSO4↓
D.铜片放入稀硝酸中产生气体:Cu+4H++2NO3﹣═ Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期10月联考化学试卷(解析版) 题型:选择题
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按右式进行:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2 由此可知,该电池充电时在阴极上发生反应的是
Cd(OH)2+2Ni(OH)2 由此可知,该电池充电时在阴极上发生反应的是
A.Ni(OH)2 B.Cd(OH)2 C.Cd D.NiOOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上学期第一次段中考试化学试卷(解析版) 题型:选择题
下列表示水解的离子方程式正确的是
A.CH3COO— + H2O CH3COOH + OH—
CH3COOH + OH—
B.NH4+ + H2O NH4OH + H+
NH4OH + H+
C.S2— + 2H2O H2S+2OH—
H2S+2OH—
D.HCO3— + H2O  H3O++CO32—
H3O++CO32—
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:填空题
Ⅰ.聚四氟乙烯在耐热性和化学稳定性上都超过了其他塑料,号称“塑料之王”,可用于制造飞机、导弹的无油轴承,密封填料,人造血管,滑雪板,不粘锅等。其合成路线如下图所示:

写出下列化学反应方程式。
B→C:_______ _________________
C→D:_____________ _
Ⅱ.实验室制取乙烯气体时,常因温度过高混合液迅速变黑,并产生具有刺激性气味的气体SO2。某同学设计了如图所示的实验装置以确证反应制得的混合气体中含有乙烯和SO2。

可供选择的试剂:①酸性高锰酸钾溶液、②稀硝酸、③浓硫酸、④品红溶液、⑤石蕊试液、⑥NaOH溶液。
(1)各装置中所盛放的试剂分别是(填写序号):A_________,B_________,C_________,D_________。
(2)装置B的作用是__________________,装置C的作用是___________________。
(3)能说明混合气体中含SO2的实验现象是_________ ______,确证混合气体中有乙烯的实验现象是____ __。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com