
关于原电池和电解池的叙述正确的是()
A. 原电池中失去电子的电极为阴极
B. 原电池的负极、电解池的阳极都发生氧化反应
C. 原电池的两极一定是由活动性不同的两种金属组成
D. 电解时电解池的阴极一定是阴离子放电
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: A、原电池中的电极为正负极不是阴阳极;
B、根据原电池负极和电解池阳极上得失电子判断反应类型;
C、原电池的两极不一定是由活动性不同的两种金属组成;
D、电解时,电解池阴极上得电子发生还原反应.
解答: 解:A、原电池中失去电子的电极为负极不是阴极,故A错误;
B、原电池负极上失电子发生氧化反应,电解池阳极上失电子发生氧化反应,故B正确;
C、原电池的两极不一定是由活动性不同的两种金属组成,可能是由金属和导电的非金属组成,故C错误;
D、电解时,电解池阴极上得电子发生还原反应,故D错误.
故选B.
点评: 本题考查了原电池和电解池原理,难度不大,注意电解时,阳极上不一定是阴离子放电,要根据电极材料判断放电物质或离子.


科目:高中化学 来源: 题型:
把200mL有BaCl2和KCl的混合溶液分成2等份,取一份加入含 A mol硫酸钾的溶液,恰好使钡离子完全沉淀;另取一份加入含 B mol硝酸银的溶液,恰好使氯离子完全沉淀.则:每份溶液中:n(Ba2+)= mol,n(Cl﹣)= mol;
200mL原混合溶液中:c(Cl﹣)= mol•L﹣1,c(K+)= mol•L﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的沸点按由高到低的顺序排列正确的是()
①CH3(CH2)2CH3②CH3(CH2)3CH3③(CH3)3CH ④(CH3)2CHCH2CH3.
A. ②④①③ B. ④②①③ C. ④③②① D. ②④③①
查看答案和解析>>
科目:高中化学 来源: 题型:
某聚合物锂离子充电电池放电时的反应为:Li1﹣xCoO2+LixC6=6C+LiCoO2,(LixC6表示锂原子嵌入石墨形成的复合材料)其工作原理如图所示,下列说法正确的是()
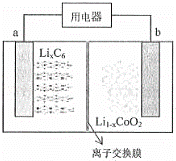
A. 放电时,电子从b极流向a极
B. 放电时,a极脱出的离子通过阴离子交换膜从左向右移动
C. 充电时,b极发生的反应为:LiCoO2﹣xe﹣=Li1﹣xCoO2+xLi+
D. 充电时,每转移x mol 电子,产生6mol碳单质
查看答案和解析>>
科目:高中化学 来源: 题型:
我国第五套人民币中的一元硬币材料为钢芯镀镍,依据你所掌握的电镀原理,你认为在硬币制作时,钢芯应做()
A. 阴极 B. 阳极 C. 正极 D. 负极
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应的△H=+122kJ•mol﹣1,△S=﹣231J•mol﹣1•K﹣1,则此反应在下列哪种情况下可自发进行()
A. 在任何温度下都能自发进行
B. 在任何温度下都不能自发进行
C. 仅在高温下自发进行
D. 仅在低温下自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
在C(固)+CO2(气)=2CO(气)的反应中.现采取下列措施:
(1)增大压强;(2)增加碳的量;(3)通入CO2;(4)恒容下充入N2;(5)恒压下充入N2,哪些措施能够使反应速率增大?()
A. (1)(3) B. (3)(5) C. (1)(2)(3) D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后()
A. 整个溶液变紫色 B. 整溶液变为棕黄色
C. 上层为无色下层为紫红色 D. 下层无色上层紫红色
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息判断,下列选项不正确的是()
序号 反应物 产物
① KMnO4、H2O2、H2SO4 K2SO4、MnSO4
② Cl2、FeBr2 FeCl3、FeBr3
③ MnO4﹣ Cl2、Mn2+
A. 第①组反应的 其余产物为H2O和O2
其余产物为H2O和O2
B. 第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
C. 第③组反应中生成1mol Cl2,转移电子2mol
D. 氧化性由强到弱顺序为MnO4﹣>Cl2>Fe3+>Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com