
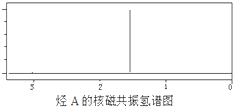
 ijĢžA¾Ąī±ČĻ£ŌŖĖŲ·ÖĪöŹµŃé²āµĆĢ¼µÄÖŹĮæ·ÖŹżĪŖ85.71%£¬øĆĢžµÄÖŹĘ×Ķ¼ĻŌŹ¾£ŗ·Ö×ÓĄė×Ó·åµÄ×ī“óÖŹŗɱČĪŖ84£¬øĆĢžµÄŗĖ“Ź²ÕńĒāĘ×ČēĶ¼ĖłŹ¾£®ŗģĶā¹āĘ×±ķĆ÷·Ö×Ó֊ƻӊĢ¼Ģ¼Ė«¼ü£¬ŅŃÖŖĻ©Ģž¾³ōŃõ×÷ÓĆ·¢Éś·“Ó¦£ŗ
ijĢžA¾Ąī±ČĻ£ŌŖĖŲ·ÖĪöŹµŃé²āµĆĢ¼µÄÖŹĮæ·ÖŹżĪŖ85.71%£¬øĆĢžµÄÖŹĘ×Ķ¼ĻŌŹ¾£ŗ·Ö×ÓĄė×Ó·åµÄ×ī“óÖŹŗɱČĪŖ84£¬øĆĢžµÄŗĖ“Ź²ÕńĒāĘ×ČēĶ¼ĖłŹ¾£®ŗģĶā¹āĘ×±ķĆ÷·Ö×Ó֊ƻӊĢ¼Ģ¼Ė«¼ü£¬ŅŃÖŖĻ©Ģž¾³ōŃõ×÷ÓĆ·¢Éś·“Ó¦£ŗ| ¢ŁO3 |
| ¢ŚH2O |
| 85.71% |
| 12 |
| 14.29% |
| 1 |
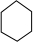 £¬ÓėĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬B·Ö×ÓÖŠÖ»ŗ¬ÓŠŅ»øöĀČŌ×Ó£¬ŌņBĪŖ
£¬ÓėĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬B·Ö×ÓÖŠÖ»ŗ¬ÓŠŅ»øöĀČŌ×Ó£¬ŌņBĪŖ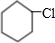 £¬B·¢ÉśĻūČ„·“Ӧɜ³ÉCĪŖ
£¬B·¢ÉśĻūČ„·“Ӧɜ³ÉCĪŖ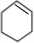 £¬C·¢ÉśŠÅĻ¢ÖŠ³ōŃõŃõ»ÆÉś³ÉDĪŖOHC£ØCH2£©4CHO£¬D·¢ÉśŃõ»Æ·“Ӧɜ³ÉEĪŖHOOC£ØCH2£©4COOH£®FÓėA×ī¼ņŹ½ĻąĶ¬£¬ĒŅFŹōÓŚĮ“דĢžÖŠ×ī¼ņµ„µÄŅ»ÖÖ£¬ŌņFĪŖCH2=CH2£¬Óėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖBrCH2CH2Br£¬G·¢ÉśĖ®½ā·“Ӧɜ³ÉHĪŖHOCH2CH2OH£¬EÓėH·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļHĪŖ
£¬C·¢ÉśŠÅĻ¢ÖŠ³ōŃõŃõ»ÆÉś³ÉDĪŖOHC£ØCH2£©4CHO£¬D·¢ÉśŃõ»Æ·“Ӧɜ³ÉEĪŖHOOC£ØCH2£©4COOH£®FÓėA×ī¼ņŹ½ĻąĶ¬£¬ĒŅFŹōÓŚĮ“דĢžÖŠ×ī¼ņµ„µÄŅ»ÖÖ£¬ŌņFĪŖCH2=CH2£¬Óėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖBrCH2CH2Br£¬G·¢ÉśĖ®½ā·“Ӧɜ³ÉHĪŖHOCH2CH2OH£¬EÓėH·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļHĪŖ £¬¾Ż“Ė½ā“š£®
£¬¾Ż“Ė½ā“š£®| 85.71% |
| 12 |
| 14.29% |
| 1 |
 £¬ÓėĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬B·Ö×ÓÖŠÖ»ŗ¬ÓŠŅ»øöĀČŌ×Ó£¬ŌņBĪŖ
£¬ÓėĀČĘų·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬B·Ö×ÓÖŠÖ»ŗ¬ÓŠŅ»øöĀČŌ×Ó£¬ŌņBĪŖ £¬B·¢ÉśĻūČ„·“Ӧɜ³ÉCĪŖ
£¬B·¢ÉśĻūČ„·“Ӧɜ³ÉCĪŖ £¬C·¢ÉśŠÅĻ¢ÖŠ³ōŃõŃõ»ÆÉś³ÉDĪŖOHC£ØCH2£©4CHO£¬D·¢ÉśŃõ»Æ·“Ӧɜ³ÉEĪŖHOOC£ØCH2£©4COOH£®FÓėA×ī¼ņŹ½ĻąĶ¬£¬ĒŅFŹōÓŚĮ“דĢžÖŠ×ī¼ņµ„µÄŅ»ÖÖ£¬ŌņFĪŖCH2=CH2£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖBrCH2CH2Br£¬G·¢ÉśĖ®½ā·“Ӧɜ³ÉHĪŖHOCH2CH2OH£¬EÓėH·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļHĪŖ
£¬C·¢ÉśŠÅĻ¢ÖŠ³ōŃõŃõ»ÆÉś³ÉDĪŖOHC£ØCH2£©4CHO£¬D·¢ÉśŃõ»Æ·“Ӧɜ³ÉEĪŖHOOC£ØCH2£©4COOH£®FÓėA×ī¼ņŹ½ĻąĶ¬£¬ĒŅFŹōÓŚĮ“דĢžÖŠ×ī¼ņµ„µÄŅ»ÖÖ£¬ŌņFĪŖCH2=CH2£¬FÓėäå·¢Éś¼Ó³É·“Ӧɜ³ÉGĪŖBrCH2CH2Br£¬G·¢ÉśĖ®½ā·“Ӧɜ³ÉHĪŖHOCH2CH2OH£¬EÓėH·¢ÉśĖõ¾Ū·“Ӧɜ³Éøß¾ŪĪļHĪŖ £¬
£¬ £¬CĪŖ
£¬CĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£» £»
£»| Ė® |
| ”÷ |
 £¬
£¬| Ė® |
| ”÷ |
 £»
£» £©µÄĮ“דĶ¬·ÖŅģ¹¹ĢåÖŠ£¬“ęŌŚĖ³·“Ņģ¹¹µÄAµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗCH3CH2CH=CHCH2CH3”¢CH3CH=CHCH2CH2CH3”¢CH3CH=CHCH£ØCH3£©2”¢CH3CH=C£ØCH3£©C2H5£¬¹Ź“š°øĪŖ£ŗ4£®
£©µÄĮ“דĶ¬·ÖŅģ¹¹ĢåÖŠ£¬“ęŌŚĖ³·“Ņģ¹¹µÄAµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗCH3CH2CH=CHCH2CH3”¢CH3CH=CHCH2CH2CH3”¢CH3CH=CHCH£ØCH3£©2”¢CH3CH=C£ØCH3£©C2H5£¬¹Ź“š°øĪŖ£ŗ4£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
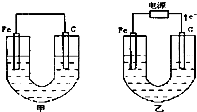 ¼×”¢ŅŅĮ½³Ųµē¼«²ÄĮĻ¶¼ŹĒĢś°ōÓėĢ¼°ō£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¼×”¢ŅŅĮ½³Ųµē¼«²ÄĮĻ¶¼ŹĒĢś°ōÓėĢ¼°ō£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ĒāŃõ»ÆĶŗĶĻ”ŃĪĖį·“Ó¦ |
| B”¢ĒāŃõ»Æ±µČÜŅŗµĪČėĻ”ĮņĖįÖŠ |
| C”¢ĒāŃõ»ÆÄĘČÜŅŗÓėĻõĖį·“Ó¦ |
| D”¢“×ĖįŗĶĒāŃõ»Æ¼ŲČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
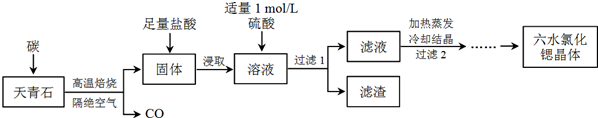
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
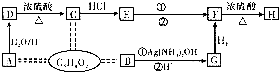
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢ŌŚŹµŃéŹŅĄļ¹čĖįÄĘČÜŅŗ“ę·ÅŌŚ“ųĻš½ŗČūµÄŹŌ¼ĮĘæÖŠ |
| B”¢Ģį³«ČĖĆĒ¹ŗĪļŹ±²»ÓĆĖÜĮĻ“ü£¬ŹĒĪŖĮĖ·ĄÖ¹°×É«ĪŪČ¾ |
| C”¢·śĄū°ŗ£ØCCl2F2£©ŅņĘĘ»µ“óĘų³ōŃõ²ć¶ųµ¼ÖĀ”°ĪĀŹŅŠ§Ó¦”± |
| D”¢ĪŖ·ĄÖ¹µē³ŲÖŠµÄÖŲ½šŹōµČĪŪČ¾ĶĮČĄŗĶĖ®Ģ壬Ӧ»ż¼«æŖ·¢·Ļµē³ŲµÄ×ŪŗĻĄūÓĆ¼¼Źõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢NaClČÜŅŗŌŚµēĮ÷µÄ×÷ÓĆĻĀµēĄė³öNa+ |
| B”¢Ąė×Ó»ÆŗĻĪļŅ»¶ØŹĒµē½āÖŹ |
| C”¢°±Ė®³ŹČõ¼īŠŌ£¬¹ŹNH3ŹĒČõµē½āÖŹ |
| D”¢ČÜÓŚĖ®µēĄė³öĒāĄė×ӵĻÆŗĻĪļ¶¼ŹĒĖį |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¢Ł¢Ū¢ß | B”¢¢Ū¢Ż |
| C”¢¢Ś¢Ū¢Ž | D”¢¢Ü¢Ž |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com