
| A. | 氨分子的电子式: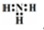 | |
| B. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| C. | O2-的结构示意图为: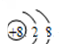 | |
| D. | ${\;}_{35}^{79}$Br的基态原子电子排布式:[Ar]4S24P5 |
分析 A.氨气分子的电子式中漏掉了氮原子的1对未成键电子;
B.质量数=质子数+中子数,该氯原子的质量数为37;
C.O2-的质子数是8,电子数是10;
D.Br元素为35号元素,原子核外有35个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p5.
解答 解:A.氨气分子中氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对孤电子对,氨气的电子式为 ,故A错误;
,故A错误;
B.质子数为17、中子数为20的氯原子的质量数为37,其正确的表示方法为:1737Cl,故B错误;
C.O2-的质子数是8,电子数是10,结构示意图为: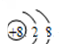 ,故C正确;
,故C正确;
D.Br元素为35号元素,原子核外有35个电子,所以核外电子排布式为:[Ar]3d104s24p5,故D错误.
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、元素符号、离子结构示意图、电子排布式等知识,明确常见化学用语的书写原则为解答结构,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 最外层电子数 | 次外层电子数 |
| D | x | x+4 |
| F | x+3 | x+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
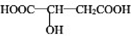 )常用于汽水、糖果的添加剂,
)常用于汽水、糖果的添加剂,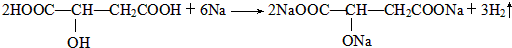 ;
;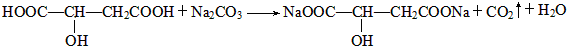
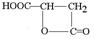 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等.
实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等.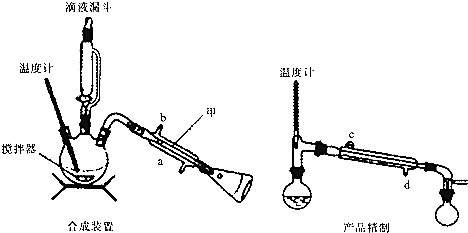
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用合适的催化剂可以增大反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 增大压强不影响反应速率 | |
| D. | 增大N2浓度可以增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:Na+、K+、SO${\;}_{4}^{2-}$、AlO${\;}_{2}^{-}$ | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-12mol•L-1的澄清溶液中:Cu2+、Mg2+、SO42-、NO${\;}_{3}^{-}$ | |
| C. | 0.1mol•L-1FeCl2溶液中:Al+、Ca2+、SCN-、ClO- | |
| D. | 水电离的c(H+)=1×10-13mol•L-1的溶液中:K+、NH${\;}_{4}^{+}$、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Al>Mg>Na | B. | 热稳定性:HF>H2O>NH3 | ||
| C. | 酸性:HClO4>H2SO4>H2PO4 | D. | 金属性:Na>Mg>Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com