
白磷在高压下隔绝空气加热后急速冷却,可得深灰色固体——黑磷,其转化过程中能量变化如图所示。下列叙述中正确的是( )

A.黑磷比白磷稳定 B.黑磷与白磷互为同分异构体
C.白磷转化为黑磷是氧化还原反应 D.白磷转化为黑磷是吸热反应
科目:高中化学 来源: 题型:
化学理论在元素单质及其化合物反应中应用广泛。
(1)在一定条件下,可逆反应mA nB+pC ⊿H,达到平衡状态。
nB+pC ⊿H,达到平衡状态。
①若A、B、C都是气体,增大压强,平衡向逆反应方向移动,则m (填“大于”、“小于”或“等于”)n+p。
②其他条件不变,加热后A的质量增加,则反应⊿H________0(填“大于”、“小于”或“等于”)。
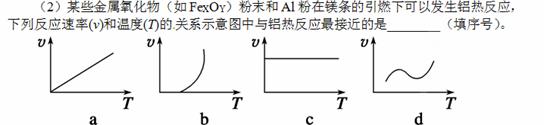 (3)一定温度下,发生反应:FeO(s)+CO(g)
(3)一定温度下,发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH。已知该反应在不同温度下的平衡常数如下表:
Fe(s)+CO2(g) ΔH。已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
请回答下列问题:
①该反应的ΔH___ 0(填“>”、“<”或“=”)。
②T℃时,将FeO(s)和CO(g)各3.0 mol加入10 L的密闭容器中,反应达到平衡后,测得CO转化率为W1,c(CO2) =0.15mol·L-1,则温度T (填“高于”、“低于”、“等于”)1000, 若此时保持其它条件不变再充入2.0 mol CO(g),再达平衡时测得CO转化率为W2,则W1 (填“>”、“<”或“=”)W2。
查看答案和解析>>
科目:高中化学 来源: 题型:
HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH  B.分别在两种溶液中滴加甲基橙
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别 D.用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:________________________ 。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝制易拉罐收集满CO2,快速加入过量NaOH浓溶液,立即把口封闭。发现易拉罐“咔咔”作响,并变瘪了:过一会儿,易拉罐又会作响并鼓起来。下列说法正确的是
A.导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3-
B.导致易拉罐又鼓起来的反应是: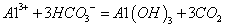
C.若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象
D.上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述中,合理的是__________
A实验室中少量金属钠、钾保存在汽油中
B容量瓶、分液漏斗、酸(碱)式滴定管等仪器在使用前都必须检验是否漏水
C圆底烧瓶、锥形瓶、烧杯加热时都应垫在石棉网上
D用一定浓度的盐酸滴定未知浓度的氢氧化钠溶液时,酸式滴定管记录起始体积时,平视读数,终点时俯视,所测碱的浓度偏高
E.不用其它化学试剂即可鉴别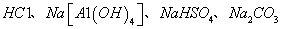 四种无色溶液
四种无色溶液
F.可以用渗析的方法除去淀粉溶液中的氯化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列装置能达到预期目的的是( )
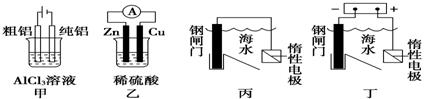
A.甲图装置可用于电解精炼铝 B.乙图装置可得到持续、稳定的电流
C.丙图装置可达到保护钢闸门的目的 D.丁图装置可达到保护钢闸门的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃下的溶液中,c(H+)=1.0×10-xmol·L-1,c(OH-)=1.0×10-ymol·L-1,x与y的关系如图所示。下列说法不正确的是( )
 A.T ℃时,水的离子积Kw为1×10-13
A.T ℃时,水的离子积Kw为1×10-13
B.T>25
C.T ℃时,pH=7的溶液显碱性
D.T ℃时,pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式书写错误的是( )
A.H2SO4= 2H+ + SO42- B.Ba(OH)2= Ba2+ + 2OH-
C.Na2CO3 =2Na+1 + CO3-2 D.NaHCO3= Na+ +HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如下:
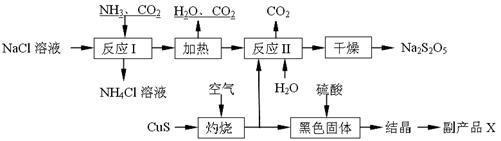
已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式: 。
(2)“灼烧”时发生反应的化学方程式: 。
(3)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为: 。
(4)副产品X的化学式是: ;可循环利用的物质是:__________________。
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约
为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com