
| A、CO2浓度不变 |
| B、正反应速率大于逆反应速率 |
| C、正反应速率等于逆反应速率 |
| D、正反应速率小于逆反应速率 |
科目:高中化学 来源: 题型:
| A、H2Y的电离方程式:H2Y?2H++Y2- |
| B、HY-的水解方程式:HY-+H2O?H3O++Y2- |
| C、该酸式盐溶液中离子浓度关系:c(Na+)>c(HY-)>c(OH-)>c(H+) |
| D、该酸式盐溶液中离子浓度关系:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和苯都能与溴水反应 |
| B、乙酸和油脂都能与氢氧化钠溶液反应 |
| C、糖类和蛋白质都是人体重要的营养物质 |
| D、乙烯和甲烷可用酸性高锰酸钾溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
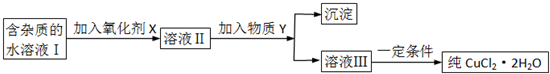
查看答案和解析>>
科目:高中化学 来源: 题型:
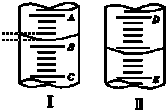 如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )
如图,图Ⅰ表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,图Ⅱ表示50mL滴定管中液面的位置,D与E刻度间相差1mL.如果刻度A和D都是4,则两处液面的读数是( )| A、Ⅰ中是3.2mL,Ⅱ中是3.40mL |
| B、Ⅰ中是4.8mL,Ⅱ中是3.40mL |
| C、Ⅰ中是3.2mL,Ⅱ中是4.60mL |
| D、Ⅰ中是4.8mL,Ⅱ中是4.60mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将混合气体通过盛有硫酸的洗气瓶 |
| B、将混合气体通过盛有足量溴水的洗气瓶 |
| C、将混合气体通过盛有酸性KMnO4溶液的洗气瓶 |
| D、将混合气体通过盛有澄清石灰水的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
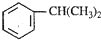 是一种重要的有机化工原料.根据题意完成下列
是一种重要的有机化工原料.根据题意完成下列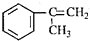 是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法
是生产耐热型ABS树脂的一种单体,工业上由异丙苯催化脱氢得到.写出由异丙苯制取该单体的另一种方法查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com