

| A.五种溶液中,水电离出的c(OH-)最小的是⑤ |
| B.将①、④两种溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)> c(OH-)。 |
| C.分别将①、②、③、④加水稀释100倍,稀释后四种溶液的pH:①>②>③>④ |
| D.在⑤中加入适量的④至溶液呈中性,所得溶液中:c(Na+)>c(CH3COO-)> c(Cl-)>c(OH-)= c(H+)。 |


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:不详 题型:单选题
| A.c(OH-) | B.pH | C.c(NH4+)/c(NH3·H2O) | D.c(H+)·c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0. 1mol/L (NH4)2SO4溶液中:c(SO42—)<c(NH4+) |
| B.相同温度下,0.6 mol/L 氨水溶液与0.3 mol/L 氨水溶液中c(OH—)之比是2:1 |
| C.向0.1 mol/L NaNO3溶液中滴加稀HNO3使溶液中pH=5,则混合溶液中c(Na+)<c(NO3—) |
| D.常温下向CH3COONa溶液中加入适量CH3COOH溶液,使混合液的pH=7,则混合液中c(Na+)<c(CH3COO—) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
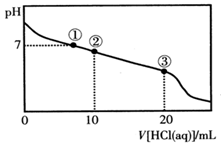
| A.点①所示溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-) |
| B.点②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) |
| C.点③所示溶液中:c(Na+)>c(CH3COOH)>c(H+)>c(CH3COO-) |
| D.整个过程中可能出现:c(H+)+c(Na+)=c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25℃时,0.1 mol·L-1HF溶液中pH=1 | B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中有CaF2沉淀产生 | D.加入CaCl2溶液后体系中的c(H+)浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | ① | ② | ③ | ④ |
| pH | 10 | 10 | 4 | 4 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
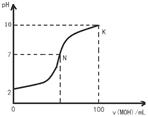
| A.MOH是弱碱 |
| B.N点c(Cl-) = c(M+) |
C.随着MOH溶液的滴加,比值 不变 不变 |
| D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=2与pH=1的CH3COOH溶液中,c(H+)之比为1 :10 |
| B.1.0mol/ L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C.仅含Na+、H+、OH-、CH3COO-离子的某溶液中可能存在: c(Na+)>c(CH3COO-) >c(OH-)>c(H+) |
| D.0.1mol/ L的CH3COOH溶液中,由水电离出的c(H+)为1×10-13mol/ L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com