
ΓΨΧβΡΩΓΩ2SO2(g)ΘΪO2(g) ![]() 2SO3(g) «ΙΛ“Β÷ΤΝρΥαΒΡ÷ς“ΣΖ¥”Π÷°“ΜΓΘ“ΜΕ®Έ¬Ε»œ¬Θ§‘ΎΦΉΓΔ““ΓΔ±ϊ»ΐΗω»ίΜΐΨυΈΣ2 LΒΡΚψ»ίΟή±’»ίΤς÷–ΆΕ»κSO2(g)ΚΆO2(g)Θ§ΤδΤπ ΦΈο÷ ΒΡΝΩΦΑSO2ΒΡΤΫΚβΉΣΜ·¬ »γœ¬±μΥυ ΨΘΚ
2SO3(g) «ΙΛ“Β÷ΤΝρΥαΒΡ÷ς“ΣΖ¥”Π÷°“ΜΓΘ“ΜΕ®Έ¬Ε»œ¬Θ§‘ΎΦΉΓΔ““ΓΔ±ϊ»ΐΗω»ίΜΐΨυΈΣ2 LΒΡΚψ»ίΟή±’»ίΤς÷–ΆΕ»κSO2(g)ΚΆO2(g)Θ§ΤδΤπ ΦΈο÷ ΒΡΝΩΦΑSO2ΒΡΤΫΚβΉΣΜ·¬ »γœ¬±μΥυ ΨΘΚ
ΦΉ | ““ | ±ϊ | ||
Τπ ΦΈο÷ ΒΡΝΩ | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | |
SO2ΒΡΤΫΚβΉΣΜ·¬ /% | 80 | ΠΝ1 | ΠΝ2 | |
œ¬Ν–≈–Εœ÷–Θ§’ΐ»ΖΒΡ «( )
AΘ°ΦΉ÷–Ζ¥”ΠΒΡΤΫΚβ≥Θ ΐ–Γ”Ύ““
BΘ°ΗΟΈ¬Ε»œ¬Θ§ΤΫΚβ≥Θ ΐ÷ΒΈΣ400
CΘ°ΤΫΚβ ±Θ§±ϊ÷–c(SO3) «ΦΉ÷–ΒΡ2±Ε
D.ΤΫΚβ ±Θ§ΦΉ÷–O2ΒΡΉΣΜ·¬ ¥σ”Ύ““÷–O2ΒΡΉΣΜ·¬
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
‘ΧβΖ÷ΈωΘΚAΘ°Έ¬Ε»œύΆ§ ±Θ§ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐ≤Μ±δΘ§‘ρΦΉΓΔ““÷–Ζ¥”ΠΒΡΤΫΚβ≥Θ ΐœύΒ»Θ§Ι A¥μΈσΘΜ
BΘ°ΗυΨί2SO2(g)+O2(g)![]() 2SO3(g)Θ§
2SO3(g)Θ§
ΩΣ Φ 0.4 0.24 0
ΉΣΜ· 0.32 0.16 0.32
ΤΫΚβ 0.08 0.08 0.32
ΤΫΚβ≈®Ε»0.04 0.04 0.16
Υυ“‘ΗΟΈ¬Ε»œ¬Θ§ΤΫΚβ≥Θ ΐ÷ΒΈΣ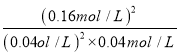 =400Θ§Ι B’ΐ»ΖΘΜCΘ°ΧεΜΐœύΆ§Θ§±ϊ÷–ΒΡΤπ Φ≈®Ε»ΈΣΦΉΒΡ2±ΕΘ§―Ι«Ω‘ω¥σΘ§ΤΫΚβ’ΐœρ“ΤΕ·Θ§‘ρ±ϊ÷–ΉΣΜ·¬ ‘ω¥σΘ§Φ¥±ϊ÷–c(SO3)¥σ”ΎΦΉ÷–c(SO3)ΒΡ2±ΕΘ§Ι C¥μΈσΘΜDΘ°”…ΦΉΓΔ““Ω…÷ΣΘ§―θΤχΒΡ≈®Ε»œύΆ§Θ§Εΰ―θΜ·ΝρΒΡ≈®Ε»‘ω¥σΜα¥ΌΫχ―θΤχΒΡΉΣΜ·Θ§‘ρ““÷–O2ΒΡΉΣΜ·¬ ¥σ”ΎΦΉ÷–O2ΒΡΉΣΜ·¬ Θ§Ι D¥μΈσΘΜΙ ―ΓBΓΘ
=400Θ§Ι B’ΐ»ΖΘΜCΘ°ΧεΜΐœύΆ§Θ§±ϊ÷–ΒΡΤπ Φ≈®Ε»ΈΣΦΉΒΡ2±ΕΘ§―Ι«Ω‘ω¥σΘ§ΤΫΚβ’ΐœρ“ΤΕ·Θ§‘ρ±ϊ÷–ΉΣΜ·¬ ‘ω¥σΘ§Φ¥±ϊ÷–c(SO3)¥σ”ΎΦΉ÷–c(SO3)ΒΡ2±ΕΘ§Ι C¥μΈσΘΜDΘ°”…ΦΉΓΔ““Ω…÷ΣΘ§―θΤχΒΡ≈®Ε»œύΆ§Θ§Εΰ―θΜ·ΝρΒΡ≈®Ε»‘ω¥σΜα¥ΌΫχ―θΤχΒΡΉΣΜ·Θ§‘ρ““÷–O2ΒΡΉΣΜ·¬ ¥σ”ΎΦΉ÷–O2ΒΡΉΣΜ·¬ Θ§Ι D¥μΈσΘΜΙ ―ΓBΓΘ


 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣAΓΔBΓΔCΓΔDΥΡ÷÷‘ΣΥΊΒΡ‘≠Ή”–ρ ΐΈΣAΘΦBΘΦCΘΦDΘ§«“ΕΦ–Γ”Ύ18ΓΘAΓΔBΈΜ”ΎΆ§÷ήΤΎΘ§A‘ΣΥΊΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒγΉ” ΐΒΡ2±ΕΘ§B‘ΣΥΊΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒγΉ” ΐΒΡ3±ΕΓΘCΓΔDΆ§÷ήΤΎΘ§ C‘ΣΥΊΒΡ‘≠Ή”ΑκΨΕ‘ΎΆ§÷ήΤΎ÷–Ήν¥σΘ§D‘ΣΥΊΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ±»¥ΈΆβ≤ψΒγΉ” ΐ…Ό1ΗωΓΘ ‘ΆΤΕœΘΚ
Θ®1Θ©«κ–¥≥ωAΓΔBΓΔCΓΔDΥΡ÷÷‘ΣΥΊΒΡ‘ΣΥΊΖϊΚ≈ΘΚA________Θ§B________Θ§C________Θ§D_______ΓΘ
Θ®2Θ©Μ≠≥ωD‘ΣΥΊΒΡάκΉ”ΫαΙΙ Ψ“βΆΦ_______________ΓΘ
Θ®3Θ©AB2÷–¥φ‘ΎΒΡΜ·―ßΦϋ « Θ®άκΉ”ΦϋΓΔΙ≤ΦέΦϋΘ©Θ§ CDΒΡΒγΉ” ΫΈΣ ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ ÷–Φ»Κ§ΦΪ–‘Ι≤ΦέΦϋ”÷Κ§”–άκΉ”ΦϋΒΡ «( )
AΘ°NaOH BΘ°KCl CΘ°HCl DΘ°H2SO4
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ―–ΨΩNO2ΓΔSO2ΓΔCOΒ»¥σΤχΈέ»ΨΤχΧεΒΡ¥ΠάμΨΏ”–÷Ί“Σ“β“εΓΘ
Θ®1Θ©“―÷ΣΘΚ2SO2(g)+O2(g) ![]() 2SO3(g) ΠΛH= -196.6kJΓΛmol-1
2SO3(g) ΠΛH= -196.6kJΓΛmol-1
2NO(g)+O2(g) ![]() 2NO2(g) ΠΛH= -113.0kJΓΛmol-1
2NO2(g) ΠΛH= -113.0kJΓΛmol-1
‘ρΖ¥”ΠNO2(g)+SO2(g) ![]() SO3(g)+NO(g)ΒΡΠΛH= kJΓΛmol-1
SO3(g)+NO(g)ΒΡΠΛH= kJΓΛmol-1
Θ®2Θ©“ΜΕ®ΧθΦΰœ¬Θ§ΫΪNO2”κSO2“‘ΧεΜΐ±»2ΓΟ1÷Ο”ΎΟή±’»ίΤς÷–ΖΔ…ζ…œ ωΖ¥”ΠΘ§œ¬Ν–ΡήΥΒΟςΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§ΒΡ «
AΘ°ΧεœΒ―Ι«Ω±Θ≥÷≤Μ±δ
BΘ°ΜλΚœΤχΧε―’…Ϊ±Θ≥÷≤Μ±δ
CΘ°SO3ΚΆNOΒΡΧεΜΐ±»±Θ≥÷≤Μ±δ
DΘ°ΟΩœϊΚΡ1molSO3ΒΡΆ§ ±…ζ≥…1mol NO
≤βΒΟ…œ ωΖ¥”Π¥οΤΫΚβ ±NO2”κSO2ΒΡΧεΜΐ±»ΈΣ5ΓΟ1Θ§‘ρΤΫΚβ≥Θ ΐK=
Θ®3Θ©COΩ…”Ο”ΎΚœ≥…ΦΉ¥ΦΘ§Ζ¥”ΠΖΫ≥Χ ΫΈΣCO(g)+2H2(g) ![]() CH3OH(g)ΓΘCO‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡΤΫΚβΉΣΜ·¬ ”κ―Ι«ΩΒΡΙΊœΒ»γΆΦΘ®2Θ©Υυ ΨΓΘΗΟΖ¥”ΠΠΛH 0(ΧνΓΑ>Γ±ΜρΓΑΘΦΓ±)ΓΘ ΒΦ …ζ≤ζΧθΦΰΩΊ÷Τ‘Ύ250ΓφΓΔ1.3ΓΝ104kPaΉσ”“Θ§―Γ‘ώ¥Υ―Ι«ΩΒΡάμ”… «ΘΚ ΓΘ
CH3OH(g)ΓΘCO‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡΤΫΚβΉΣΜ·¬ ”κ―Ι«ΩΒΡΙΊœΒ»γΆΦΘ®2Θ©Υυ ΨΓΘΗΟΖ¥”ΠΠΛH 0(ΧνΓΑ>Γ±ΜρΓΑΘΦΓ±)ΓΘ ΒΦ …ζ≤ζΧθΦΰΩΊ÷Τ‘Ύ250ΓφΓΔ1.3ΓΝ104kPaΉσ”“Θ§―Γ‘ώ¥Υ―Ι«ΩΒΡάμ”… «ΘΚ ΓΘ

Θ®4Θ©“άΨί»Φ…’ΒΡΖ¥”Π‘≠άμΘ§Κœ≥…ΒΡΦΉ¥ΦΩ…“‘…ηΦΤ»γΆΦΘ®3Θ©Υυ ΨΒΡ‘≠Βγ≥ΊΉΑ÷ΟΓΘ
ΔΌΗΟΒγ≥ΊΙΛΉς ±Θ§OH-œρ ΦΪ“ΤΕ·(ΧνΓΑ’ΐΓ±ΜρΓΑΗΚΓ±)ΓΘ
ΔΎΗΟΒγ≥Ί’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «Θ® Θ©
A. s«χΕΦ «Ϋπ τ‘ΣΥΊ B. Υυ”–Ζ«Ϋπ τ‘ΣΥΊΕΦ‘Ύp«χ
C. œΓ”–ΤχΧε‘Ύds«χ D. s«χΕΦ «÷ςΉε‘ΣΥΊ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΊ”ΎάκΉ”ΦϋΓΔΙ≤ΦέΦϋΒΡΗς÷÷–π ω÷–Θ§œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ « Θ® Θ©
AΘ°‘ΎάκΉ”Μ·ΚœΈοάοΘ§÷Μ¥φ‘ΎάκΉ”ΦϋΘ§ΟΜ”–Ι≤ΦέΦϋ
BΘ°Ζ«ΦΪ–‘Φϋ÷Μ¥φ‘Ύ”ΎΥΪ‘≠Ή”ΒΡΒΞ÷ Ζ÷Ή”Θ®»γCl2Θ©÷–
CΘ°‘ΎΙ≤ΦέΜ·ΚœΈοΖ÷Ή”ΡΎΘ§“ΜΕ®≤Μ¥φ‘ΎάκΉ”Φϋ
DΘ°”…≤ΜΆ§‘ΣΥΊΉι≥…ΒΡΕύ‘≠Ή”Ζ÷Ή”άοΘ§“ΜΕ®÷Μ¥φ‘ΎΦΪ–‘Φϋ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ –≥Γ…œ”–“Μ÷÷”Ο”Ύ‘ΛΖάΚΆ÷ΈΝΤ»±―θ÷ΔΉ¥ΒΡ±ψ–· Ϋ÷Τ―θΤςΘ§άϊ”ΟΙΐΧΦΥαΡΤΙΧΧεA(Μ·―ß ΫΈΣ2Na2CO3ΓΛ3H2O2)ΚΆΚΎ…ΪΙΧΧεB(≤Μ»ή”ΎΥ°)”κΥ°ΜλΚœΖ¥”Π÷ΤΒΟ―θΤχΓΘΡ≥Ά§―ßΕ‘AΓΔBΝΫ÷÷Έο÷ Ϋχ––ΧΫΨΩ, Β―ι≤Ϋ÷ηΦΑœ÷œσ»γœ¬ΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©

AΘ°B‘ΎΖ¥”ΠΔΌ÷–Ω…ΡήΤπ¥ΏΜ·Ής”Ο B. …ηΦΤΔέΒΡΡΩΒΡ «÷Τ»Γ―θΤχ
CΘ°ΒΎΔΎ≤ΫΖ÷άκΜλΚœΈοΒΡΖΫΖ® «ΫαΨß D. ΑΉ…Ϊ≥ΝΒμDΈΣCaCO3
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”ΟVSEPRΡΘ–Ά‘Λ≤βœ¬Ν–Ζ÷Ή”ΜράκΉ”ΒΡΝΔΧεΫαΙΙΘ§Τδ÷–’ΐ»ΖΒΡ «
AΘ°H2O”κBeCl2ΈΣV–Έ
BΘ°CS2”κSO2ΈΣ÷±œΏ–Έ
CΘ°BF3”κPCl3ΈΣ»ΐΫ«ΉΕ–Έ
DΘ°SO3”κCOΈΣΤΫΟφ»ΐΫ«–Έ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
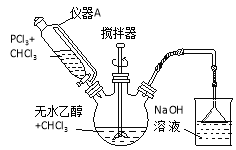
ΓΨΧβΡΩΓΩ―«ΝΉΥαΕΰ““θΞ[HPO(OC2H5)2]ΈΣ÷Ί“ΣΒΡΉη»Φ‘ωΥήΦΝΓΘ Β―ι “≤…”Ο»ΐ¬»Μ·ΝΉΚΆΈόΥ°““¥Φ÷Τ±Η―«ΝΉΥαΕΰ““θΞPCl3 + 4C2H5OH Γζ HPO(OC2H5)2 + HClΓϋ+2C2H5Cl + H2OΘΜ Β―ι≤Ϋ÷η»γœ¬ΘΚ
ΔΌΫΪ40mL»ΐ¬»ΦΉΆιΚΆ36.8g(0.8mol)ΈόΥ°““¥ΦΜλΚœΚσΦ”»κ250mL»ΐΨ±…’ΤΩ÷–ΓΘ
ΔΎ¥”“«ΤςA÷–ΒΈΦ”20mL»ΐ¬»ΦΉΆιΚΆ27.5g (0.2mol)PCl3ΜλΚœ»ή“ΚΘ§”Ο±υΥ°ΩΊΈ¬6ΓΪ8ΓφΘ§ΩΣΕ·ΫΝΑηΤςΘ§‘Φ1hΒΈΦ”Άξ±œΓΘ
ΔέΫΪΖ¥”ΠΈοΒΙ»κ…’±≠÷–Θ§”Ο10%ΒΡΧΦΥαΡΤ»ή“Κ÷–ΚΆ÷ΝpHΈΣ7ΓΪ8Θ§‘Ό”Ο»ΞάκΉ”Υ°œ¥Β”»ΐ¥ΈΘ§‘Ύ“«ΤςB÷–Ζ÷άκΓΘ
ΔήΦθ―Ι’τΝσΘ§ ’Φ·≤ζΤΖΘ§ΒΟ23.32g≤ζΤΖΓΘ
Θ®1Θ©ΉΑ÷ΟΆΦ÷–“«ΤςAΫ–ΉωΚψ―ΙΒΈ“Κ¬©ΕΖΘ§”κΖ÷“Κ¬©ΕΖ±»Θ§ΒΈ“Κ ±ΒΡ”≈Βψ « ΘΜ≤Ϋ÷ηΔέ÷–“«ΤςBΟϊ≥ΤΈΣ ΓΘΆΦ÷–NaOH»ή“ΚΒΡΉς”ΟΈΣ ΓΘ
Θ®2Θ©”ΟΧΦΥαΡΤ»ή“Κœ¥Β”ΒΡΡΩΒΡ « ΘΜ”Ο»ΞάκΉ”Υ°œ¥Β”ΒΡΡΩΒΡ « ΓΘ
Θ®3Θ©Φθ―Ι’τΝσ≥ΐΒΟΒΫ≤ζΤΖΆβΜΙΩ…ΜΊ ’ΒΡ”–ΜζΈο”– Θ®–¥ΝΫΗωΒΡΫαΙΙΦρ ΫΘ©ΓΘ
Θ®4Θ©¥”ΈόΥ°““¥Φάϊ”ΟΫ«Ε»ΦΤΥψΘ§±Ψ¥Έ Β―ι≤ζ¬ ΈΣ Θ®Χν ΐ÷ΒΘ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com