
【题目】喷泉是一种常见的自然现象,其产生原因是存在压强差。

(1)图甲中,为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中盛有液体。
①下列组合中不可能形成喷泉的是(______)。
A.HCl和H2O B.O2和H2O C.NH3和H2O D.CO2和NaOH溶液 E.NO2和H2O
②若用D组合做喷泉实验,烧杯中的液体一定是NaOH溶液吗________?
③用A组合做喷泉实验时,若烧瓶中充满HCl气体,则在标准状况下,做完实验后烧瓶中c(HCl)=________mol·L-1(设溶质不扩散)。
④若用E组合做喷泉实验时,则标准状况下,做完实验后烧瓶中溶质的物质的量浓度是________mol·L-1。
(2)某学生积极思考产生喷泉的其他办法,并设计了如图乙所示的装置。
①在图乙的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是(______)
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
这种方法产生喷泉的原理是__________________。
②在图乙锥形瓶外放一水槽,瓶中加入酒精,水槽中加入水后,再加入足量的下列物质,结果也产生喷泉。水槽中加入的物质可以是________这种方法产生喷泉的原理是_____________________________________________________。
A.浓硫酸 B.食盐 C.硝酸钾 D.硫酸铜
③比较图甲和图乙两套装置,从产生喷泉的原理来分析,图甲________上部烧瓶内气体压强;图乙________下部锥形瓶内气体压强(填“增大”或“减小”)。
(3)城市中常见的人造喷泉及火山爆发的原理与上述________(填“图甲”或“图乙”)装置的原理相似。
【答案】B 不一定,只要胶头滴管中盛有足够的浓碱溶液足以把烧瓶中的CO2吸收即可 ![]()
![]() D 锥形瓶中发生反应:NH4HCO3+HCl=NH4Cl+CO2↑+H2O,随着CO2气体的产生,锥形瓶中的压强增大而产生“喷泉” A 浓H2SO4溶于水时,放出大量的热,温度升高使锥形瓶中的酒精挥发加快,瓶内压强增大,从而形成“喷泉” 减小 增大 图乙
D 锥形瓶中发生反应:NH4HCO3+HCl=NH4Cl+CO2↑+H2O,随着CO2气体的产生,锥形瓶中的压强增大而产生“喷泉” A 浓H2SO4溶于水时,放出大量的热,温度升高使锥形瓶中的酒精挥发加快,瓶内压强增大,从而形成“喷泉” 减小 增大 图乙
【解析】
(1)①A.HCl极易溶于H2O,可在烧瓶内形成负压,从而产生喷泉,A不合题意;
B.O2不易溶于H2O,在烧瓶内不能形成负压,不产生喷泉,B符合题意;
C.NH3极易溶于H2O,可使烧瓶内压强减小,从而产生喷泉,C不合题意;
D.CO2易溶于NaOH溶液,可在烧瓶内形成负压,从而产生喷泉,D不合题意;
E.NO2与H2O反应,可使烧瓶内气压减小,从而产生喷泉,E不合题意。答案为:B;
②若用D组合做喷泉实验,烧杯中的液体不一定是NaOH溶液。答案为:不一定,只要胶头滴管中盛有足够的浓碱溶液足以把烧瓶中的CO2吸收即可;
③用A组合做喷泉实验时,若烧瓶中充满HCl气体,做完实验后烧瓶中溶液的体积等于气体的体积,则c(HCl)= =
=![]() mol·L-1。答案为:
mol·L-1。答案为:![]() ;
;
④若用E组合做喷泉实验时,二氧化氮溶于水发生反应:3NO2+H2O=2HNO3+NO,所得溶液是硝酸溶液,做完实验后烧瓶中溶液的体积是烧瓶体积的![]() ,则溶质的物质的量浓度是
,则溶质的物质的量浓度是 =
=![]() mol·L-1。答案为:
mol·L-1。答案为:![]() ;
;
(2)①A.Cu与稀盐酸不反应,不能产生气体,A不合题意;
B.NaHCO3与NaOH溶液反应,但不产生气体,不能将锥形瓶内的液体压入烧瓶内,B不合题意;
C.CaCO3与稀硫酸不能持续反应,不能产生能将锥形瓶内的液体压入烧瓶内的气体,C不合题意;
D.NH4HCO3与稀盐酸反应,生成CO2气体,可将锥形瓶内的液体压入烧瓶内,D符合题意。答案为:D;
这种方法产生喷泉的原理是锥形瓶中发生反应:NH4HCO3+HCl=NH4Cl+CO2↑+H2O,随着CO2气体的产生,锥形瓶中的压强增大而产生“喷泉”。答案为:锥形瓶中发生反应:NH4HCO3+HCl=NH4Cl+CO2↑+H2O,随着CO2气体的产生,锥形瓶中的压强增大而产生“喷泉”;
②水槽中加入的物质可以是A,这种方法产生喷泉的原理浓H2SO4溶于水时,放出大量的热,温度升高使锥形瓶中的酒精挥发加快,瓶内压强增大,从而形成“喷泉”。答案为:A;浓H2SO4溶于水时,放出大量的热,温度升高使锥形瓶中的酒精挥发加快,瓶内压强增大,从而形成“喷泉”;
③比较图甲和图乙两套装置,从产生喷泉的原理来分析,图甲减小上部烧瓶内气体压强;图乙增大下部锥形瓶内气体压强。答案为:减小;增大;
(3)城市中常见的人造喷泉及火山爆发的原理与上述图乙装置的原理相似。答案为:图乙。


科目:高中化学 来源: 题型:
【题目】下列与金属腐蚀有关的说法,正确的是( )
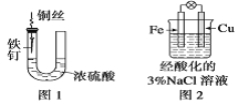
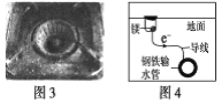
A.图1中,铁钉易被腐蚀
B.图2中,滴加少量K3[Fe(CN)6]溶液,没有蓝色沉淀出现
C.图3中,燃气灶的中心部位容易生锈,主要是由于高温下铁发生化学腐蚀
D、图4中,用牺牲镁块的方法来防止地下钢铁管道的腐蚀,镁块相当于原电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合溶液中,各离子浓度的大小顺序正确的是
A. 10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合:c(Cl)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(Cl)>c(OH)>c(H+)
C. 10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合:c(Na+)=c(CH3COO)>c(OH)>c(H+)
D. 10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl)>c(Na+)>c(OH)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。
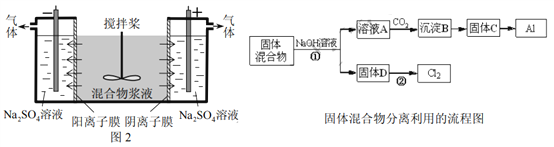
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________,B→C的反应条件为__________,C→Al的制备方法称为______________。
(2)该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化;加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___________。
a.温度 b.Cl-的浓度 c.溶液的酸度
(3)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
Ⅱ.含铬元素溶液的分离和利用
(4)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000 mol·L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列说法不正确的是
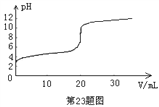
A. 在反应过程中,c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-)
B. pH=5时,c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
C. pH=6时,c(Na+)+ c(H+)-c(OH-)+ c(CH3COOH)=0.1000 mol·Lˉ1
D. pH=7时,消耗NaOH溶液的体积小于20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是
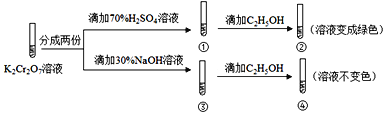
A. ①中溶液橙色加深,③中溶液变黄
B. ②中Cr2O72-被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性强
D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,利用海水可提取很多重要的化工原料。
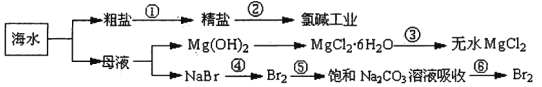
下列有关说法正确的是.( )。
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置
C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2
D.在第④步中溴元素被氧化,第⑤、⑥步中既有溴元素被氧化也有溴元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作、现象和目的或结论的说法正确的是( )
选项 | 操作 | 目的或结论 |
A | 将Fe(NO3)2晶体溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变化 | 检验Fe(NO3)2样品是否已被氧化而变质 |
B | 海带提碘实验中,为了制取海带灰的浸取液,需要煮沸海带灰和水的混合物1-2min | 主要目的是去除溶液中的氧气,避免氧气氧化碘离子 |
C | 在试管中依次加入2mL浓硫酸、3mL乙醇和2mL乙酸,用酒精灯缓慢加热 | 制备乙酸乙酯 |
D | 向盛有少量Mg(OH)2固体的试管中加入适量NH4Cl浓溶液,充分震荡,白色固体溶解 | NH4+与Mg(OH)2溶解出的OH-结合,导致Mg(OH)2溶解 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组进行铁矿石中含铁量的测定,实验过程如图:
![]()
下列说法正确的是( )
A.加热煮沸的主要目的是除去溶液中溶解的氧气
B.稀释过程中用到的玻璃仪器主要有烧杯、玻璃棒、胶头滴管
C.滴定过程中可用淀粉溶液作指示剂
D.铁矿石中铁的质量分数为70%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com