

| A. | t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲 | |
| B. | t2℃时,甲、丙两种物质的溶液中溶质的质量分数相等 | |
| C. | 若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲 | |
| D. | 若要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂的方法 |
分析 A、根据溶解度曲线图解答;
B、t2℃时甲、丙两种物质的溶解度相等,因此甲、丙两种物质的饱和溶液中溶质质量分数相等,但如果不是饱和溶液则不一定相等解答;
C、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而变化较小解答;
D、曲线上的点所对应的溶液为此温度下恰好饱和的饱和溶液,而曲线下方的点则为此时的不饱和溶液.根据溶解度受温度的变化情况,可以判断要将组成在N点的A溶液转变为M点的溶液采取的方法.
解答 解:A、根据溶解度曲线图可知,t1℃时,三种物质的溶解度大小顺序为:丙>乙>甲,故A正确;
B、在t2℃时,甲、丙两种物质的溶解度相等,因此甲、丙两种物质的饱和溶液中溶质质量分数相等,但如果不是饱和溶液则不一定相等,故B错误;
C、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而变化较小,当甲中含少量乙时,可用降温结晶的方法提纯甲,故C正确;
D、甲物质的溶解度随温度的升高而增大,所以要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂或添加溶质的方法,故D正确.
故选B.
点评 本题主要考查了固体物质的溶解度曲线的意义及根据固体物质的溶解度曲线解决相关的问题,培养学生对知识的应用能力,题目难度中等.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | 放热 1940 kJ | B. | 吸热 1940 kJ | C. | 放热 485 kJ | D. | 吸热 485 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
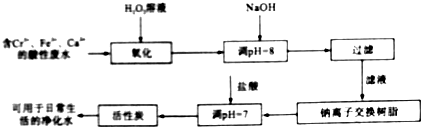
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2p能级上只有1个空轨道的原子和3p能级上只有1个空轨道的原子 | |
| B. | 最外层电子排布为3s2的原子和最外层电子排布为4s2的原子 | |
| C. | 最外层电子排布为ns2的原子和最外层电子排布为ns2np6的原子 | |
| D. | 2p能级上有2个未成对电子的原子和3p能级上有2个未成对电子的原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com