
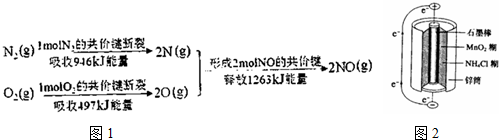
分析 (1)根据能量变化图计算反应热,反应焓变=反应物的键能和-生成物的键能和;
(2)①根据反应速率的定义进行计算;
②化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论;
(3)锌锰干电池的负极上Zn失去电子,负极消耗1mol时转移2mol电子,NH4+离子在正极放电产生2种气体,其中一种气体分子是含10e-的微粒为氨气,另一种为氢气.
解答 解:(1)由图可知,该NO分解为N2和O2的反应中的反应热=反应物的键能和-生成物的键能和=1263kJ/mol-(946+497)kJ/mol=-180kJ/mol,则该NO分解为N2和O2的反应为放热反应;
故答案为:放热;
(2)①NO2(g)+CO(g)?CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.2mol,则CO2的物质的量为0.2mol,
故v(CO2)=$\frac{\frac{△n}{V}}{t}$=$\frac{\frac{0.2}{2}}{2}$=0.05 mol•(L•min)-1,
故答案为:0.05 mol•(L•min)-1;
②A.容器内的气体反应前后遵循质量守恒,容器内气体的质量保持不变,不一定是平衡状态,故A错误;
B.NO2的物质的量浓度不再改变是平衡状态,故B正确;
C.NO2的消耗速率与CO2的消耗速率相等,说明正逆反应速率相等,是平衡状态,故C正确;
D.反应是一个前后体积不变的反应,容器内气体的物质的量保持不变,不一定是平衡状态,故D错误;
故答案为:BC;
(3)锌锰干电池的负极上Zn失去电子,负极反应为Zn-2e-═Zn2+,负极消耗1mol时转移2mol电子,每通过0.4mole-,负极质量减少0.2mol×65g/mol=13.0g,由NH4+离子在正极放电产生2种气体,其中一种气体分子是含10e-的微粒为氨气,另一种为氢气,正极反应为2NH4++2e-═2NH3↑+H2↑,
故答案为:13.0;2NH4++2e-═2NH3↑+H2↑.
点评 本题考查反应速率的计算、化学平衡的标志,电极方程式的书写以及根据图象分析判断和依据键能计算反应焓变的知识熟练掌握,综合性较强,难度较大.


科目:高中化学 来源: 题型:选择题
| 压强 A转化率 温度 | P1(MPa) | P2(MPa) |
| 400℃ | 96 | 99 |
| 500℃ | 96 | 97 |
| A. |  | B. | 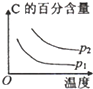 | C. |  | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 烧杯中盛有NaHSO4和Na2SO4混合溶液体积为100mL,向烧杯中逐滴加入0.15mol•L-1Ba(OH)2溶液,当沉淀量达到最大值时,溶液的总体积为200mL.溶液中产生沉淀的物质的量n与溶液的pH的变化如图所示.请回答:
烧杯中盛有NaHSO4和Na2SO4混合溶液体积为100mL,向烧杯中逐滴加入0.15mol•L-1Ba(OH)2溶液,当沉淀量达到最大值时,溶液的总体积为200mL.溶液中产生沉淀的物质的量n与溶液的pH的变化如图所示.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
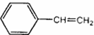 ,它不可能具有的性质是( )
,它不可能具有的性质是( )| A. | 既能使溴水褪色,也能使酸性KMnO4溶液褪色 | |
| B. | 易溶于水和有机溶剂 | |
| C. | 能与H2在一定条件下发生反应 | |
| D. | 能发生加聚反应,生成物可用 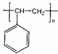 表示 表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| B. | 向石灰水中加入过量小办打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| C. | 向Ca(ClO)2中通放少量CO2:2ClO -+CO2+H2O=2HClO+CO32- | |
| D. | 用稀硝酸除去试管内壁的银镜:Ag+NO3-+2H+=Ag++NO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是非极性分子 | B. | 中心原子都采取sp杂化 | ||
| C. | S原子和C原子都没有孤对电子 | D. | SO2为V形结构,CO2为直线形结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1291℃ | 190℃ | 2073℃ | -107℃ | -57℃ | 1723℃ |
| A. | 含有金属阳离子的晶体不一定是离子晶体 | |
| B. | 同族元素的氧化物可形成不同类型的晶体 | |
| C. | 活泼金属元素与活泼非金属元素一定能形成离子化合物 | |
| D. | 金属晶体的熔点不一定比分子晶体的高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com