
小林同学发现铜制眼镜框表面出现了绿色物质,通过化学学习知道该物质为铜锈,俗称铜绿,主要成分是Cu2(OH)2CO3。
提出问题:铜是在什么条件下被锈蚀的?小林对此进行了探究。
猜想:根据铜锈的化学式,猜想铜生锈可能是铜与_____ ___作用的结果。
设计与实验:借鉴“铁钉锈蚀条件的探究”实验,小林设计了“铜片锈蚀条
件的探究”。实验如下图所示。

(1)实验较长时间后发现______________试管中的光亮铜片最先生锈。
(2)从优化实验的角度考虑,A实验是多余的,他只考虑了水这个单一条件。C试管中除光亮铜片、蒸馏水外,还有的另外一种物质为______________。
评价与改进:如果认为小林设计的“铜片锈蚀条件的探究”实验不够完善,
要得出正确的结论,还要补充的一个实验是(可画图表示)____________________。
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附中高一上期中化学卷(解析版) 题型:推断题
(1)已知4℃时四种化合物在水中和液氨中的溶解度如下表:
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O(l) | 170g | 9.20g | 1.50×10-4g | 33.3g |
NH3(l) | 86.0g | 97.2g | 0.80g | 0.01g |
①上述四种物质能在水中发生的复分解反应的离子方程式为 ;
②上述四种物质能在液氨中发生的复分解反应的化学方程式为 ;
(2)完成下列反应的离子方程式:
①碳酸氢铵溶液与少量的烧碱溶液反应: ;
②20毫升0.1mol/L碳酸氢钙溶液与56毫升0.05mol/L氢氧化钠溶液反应: ;
③石灰乳与少量的碳酸氢钠溶液反应: ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建厦门一中高一上期中考试化学试卷(解析版) 题型:选择题
某实验室合成了一种可溶的金属氯化物(RClx),为了测定该金属氯化物的成分,研究人员做了以下实验:取物质的量浓度为0.05 mol·L-1的金属氯化物(RClx) 溶液20 mL,使之恰好与20 mL 0.15 mol·L-1的AgNO3溶液完全反应。则该氯化物的化学式为
A.RCl B.RCl2 C.RCl3 D.RCl4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京顺义牛栏山一中高一上期中化学试卷(解析版) 题型:选择题
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
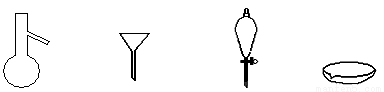
A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发
C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上期中测试化学试卷(解析版) 题型:实验题
某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入高锰酸钾溶液时,溶液褪色总是先慢后快.即反应速率由小变大.为此,甲同学做了如下实验进行探究:
(已知:MnO4-在酸性环境下的还原产物是Mn2+ )
【实验用品】仪器:试管(若干个)、胶头滴管、100mL容量瓶、250mL容量瓶、10mL量筒、托盘天平、玻璃棒、烧杯、药匙
(1)0.10mol/L H2C2O4溶液的配制:
实验室欲配制100mL 0.10mol/L H2C2O4溶液,需要称取草酸晶体(H2C2O4·2H2O) g(精确到0.1g);实验中需要用到的玻璃仪器有:玻璃棒、烧杯、胶头滴管和 .
(2)反应的速率变化的探究:
在1号和2号试管中分别加入2mL0.10mol/L H2C2O4溶液,在1号试管中加入硫酸锰固体.然后在两支试管中加入4mL 0.010mol/L KMnO4溶液和几滴稀硫酸.现象如下表所示:
试管1 | 试管2 | |
实验现象 | 褪色很快 | 褪色很慢 |
褪色时间/s | 4秒 | 31秒 |
请回答下列问题:
①甲同学进行该实验还缺少的实验仪器是: .
②H2C2O4溶液与酸性的KMnO4溶液反应的离子方程式为: .
③同学测出的颜色变化的时间是以下列哪个选项为依据的 .
A、从KMnO4溶液刚好接触H2C2O4溶液开始,溶液由紫红色变为近乎无色,半分钟之内不再出现紫 红色为止.
B、从KMnO4溶液刚好接触H2C2O4溶液开始,溶液由无色变为紫红色为止.
C、从KMnO4溶液接触H2C2O4溶液开始,溶液由紫红色变为近乎无色为止.
④甲同学认为该反应褪色由慢到快的原因是 .
于是甲同学得出结论 .
(3)乙同学和丙同学从甲同学的实验探究中得到启示,他们也分别提出了能影响该溶液化学反应速率 因素的另外两种可能原因,你认为他们提出的两种可能原因是:
I II
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上期中测试化学试卷(解析版) 题型:选择题
2g AO32-的核外电子数比质子数多3.01×1022个,则A的相对原子质量为
A.12 B.32 C.60 D.80
查看答案和解析>>
科目:高中化学 来源:2015-2016学年陕西省高二上10月月考化学试卷(解析版) 题型:选择题
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、
KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如右图。据图分析,下列判断不正确的是
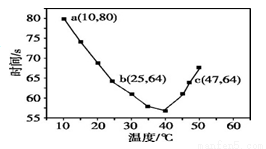
A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中a点对应的NaHSO3反应速率为5.0×10-5 mol·L-1·s-1
C.图中b、c两点对应的NaHSO3反应速率相等
D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中(理)化学试卷(解析版) 题型:实验题
用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取烧碱样2.50g,将样品配成250mL的待测液。
(2)滴定管使用前除洗涤外,还应 。
(3)取10.00mL待测液,用 量取注入锥形瓶中。(填仪器)
(4)用0.2000mol/L标准盐酸溶液滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视 直到滴定终点。
(5)根据下列测定数据,分析得到合理数据,计算待测烧碱溶液的浓度: 。
滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 10.40 |
第二次 | 10.00 | 4.00 | 14.10 |
第三次 | 10.00 | 4.20 | 15.70 |
(6)根据上述测定数据,分析得到合理数据,计算烧碱的纯度 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中(文)化学试卷(解析版) 题型:选择题
为了检验某氯化亚铁溶液是否变质,最好向溶液中加入
A.NaOH溶液 B.铁片 C.KSCN溶液 D.石蕊试液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com