
(14分)某研究性学习小组进行了如下实验探究:将适量1.00 mol·L-1 CuSO4溶液和2.00 mol·L-1 NaOH溶液混合,过滤后得到浅绿色碱式盐沉淀A[化学式:aCu(OH)2.CuSO4]。将9.08 g A隔绝空气在1 000℃左右强热,得到了5.76 g砖红色固体B(铜的+1价氧化物),同时得到的混合气体C;再将5.76 g B溶于过量稀硫酸得到2.56 g另一种红色固体D和蓝色溶液。
(1)实验需用1.00 mol·L-1 CuSO4溶液480ml,配制以上溶液需用的玻璃仪器除了烧杯、玻璃棒、量筒外还需_________________________;所称取的胆矾固体是____________;配制溶液浓度会导致所配溶液浓度偏高的是_______________
A.称量质量正确,但胆矾晶体部分失结晶水
B.配制溶液时,定容时仰视容量瓶刻度线
C.定容摇匀后发现液面低于刻度线,再往容量瓶里加水定容至刻度
D.称量胆矾时把胆矾放在右盘称
(2)B与稀硫酸反应的化学方程式为________________________________________。
(3)甲同学认为A中可能含有杂质Na+,验证此判断正确的方法是______________。
(4)气体C的成分:__________________________(SO3和SO2不需填)。
(5)通过计算确定A的组成为________________________________________________。
(14分). (1)500ml容量瓶 胶头滴管(2分) 125.0 g(2分) A(2分)
(2)Cu2O+H2SO4 = Cu + CuSO4+H2O(2分)
(3)做焰色实验,若观察到黄色火焰,则含钠离子,否则不含;(2分)
(4) O2 、H2O(2分)
(5) 3Cu(OH)2·CuSO4或Cu4(OH)6SO4(2分)
【解析】
试题分析:(1)需要480mL的溶液,需配制500mL的溶液,所以还需要500mL的容量瓶;500mL硫酸铜溶液中硫酸铜的物质的量是0.5mol,则胆矾的物质的量是0.5mol,所以胆矾的质量是0.5mol×250g/mol=125.0g;A、称量的质量正确,但胆矾失去结晶水,则胆矾中硫酸铜的物质的量会偏大,造成所配溶液浓度偏高;B、配制溶液时,定容时仰视容量瓶刻度线,会使所配溶液的体积大于500mL,溶液浓度偏低;C、定容摇匀后发现液面低于刻度线,再往容量瓶里加水定容至刻度,使溶液体积大于500mL,溶液浓度偏低;D、称量胆矾时把胆矾放在右盘称,则胆矾的质量小于125.0g,溶液浓度偏低,答案选A;
(2)砖红色固体是氧化亚铜,与稀硫酸反应生成红色固体是铜单质,和蓝色溶液为硫酸铜,所以氧化亚铜与硫酸反应的化学方程式为Cu2O+H2SO4 = Cu + CuSO4+H2O;
(3)是否含有钠离子,可作焰色反应实验,若焰色反应为黄色,证明含有钠离子,否则不含有钠离子;
(4)根据氧化还原反应理论,铜元素的化合价反应后降低,则有其他元素的化合价升高,对于S元素,化合价不能再升高,所以可以升高的元素是O,因此气体C中含有O2,在根据元素守恒,判断该气体C中应有水蒸气;
(5)9.08gA加热得到5.76gCu2O,根据铜元素守恒,9.08gA中含有的铜元素的物质的量为:5.76g/144g/mol×2=0.08mol,则9.08g/(98a+160)g/mol×(a+1)=0.08mol,解得:a=3,所以A的化学式为:3Cu(OH)2?CuSO4.
考点:考查溶液的配制,化学方程式的书写,物质化学式的计算,误差分析


科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
关于下列说法:①Fe(OH)3胶体和CuSO4溶液都是混合物;②BaSO4是一种难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④太阳能、氢能和海洋能都属于新能源;⑤置换反应都属于离子反应。其中正确的是
A.①②④ B.①②⑤ C.②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2015届江西省南昌市三校高三上第一次联考化学试卷(解析版) 题型:选择题
由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为
A.29 :8 :13 B.22 :1 :14 C.13 :8 :29 D.26 :15 :57
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次考试化学试卷(解析版) 题型:选择题
一定能在下列溶液中大量共存的离子组是
①含有大量Al3+的溶液中:Na+、NH4+、SO42—、Cl-
②加入Al能放出H2的溶液中:Cl-、HCO3—、SO42—、NH4+
③含有大量Fe3+的溶液中:Na+、Mg2+、NO3—、SCN-
④在含有大量AlO2—的溶液中:NH4+、Na+、Cl-、H+
⑤由水电离出的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3—
A.①② B.①③⑤ C.① D.①④⑤
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次考试化学试卷(解析版) 题型:选择题
利用实验器材(规格和数量不限)能完成相应实验的一项是
选项 | 实验器材(省略夹持装置) | 相应实验 l |
A | 三脚架、泥三角、坩埚、坩埚钳 | 用CuSO4 |
B | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用浓盐酸配制0.1mol·L-1的HCl溶液 |
C | 烧杯、玻璃棒、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
选项 | 叙述I | 叙述II |
A | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |
B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
D | NH4Cl为强酸弱碱盐 | 加热可除去NaCl中的NH4Cl |
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO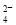 的物质的量浓度为( )
的物质的量浓度为( )
A.0.4 mol·L-1B.0.3mol·L-1C.0.2 mol·L-1D.0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江西五校高三第一次联考化学试卷(解析版) 题型:选择题
甲、乙两个电解池均以Pt为电极且互相串联。甲池盛有AgNO3溶液,乙池盛有一定量的某盐溶液,通电一段时间后,测得甲池阴极质量增加2.16g,乙池电极析出0.24g金属,则乙池中溶质可能是
A.CuSO4B.MgSO4 C.Al(NO3)3D.Na2SO4
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
COCl2(g) CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0 当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是
A.①②④ B.①④⑥ C.②③⑥ D.③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com