
SF6是一种优良的绝缘气体,分子结构中只存在S—F键。已知:1 mol S(s)转化为气态硫原子吸收能量280 kJ,断裂1 mol F—F、S—F键需吸收的能量分别为160 kJ、330 kJ。则S(s)+3F2(g)===SF6(g)的反应热ΔH为( )
A.-1 780 kJ/mol B.-1 220 kJ/mol
C.-450 kJ/mol D.+430 kJ/mol
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.碳酸氢镁溶液加入过量氢氧化钠: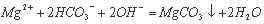
B.碳酸钡溶于醋酸溶液: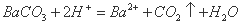
C.次氯酸钙溶液中通入少量二氧化碳: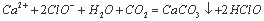
D.氧化铁加入氢碘酸中: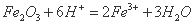
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是( )
A.W2-、X+ B.X+、Y3+
C.Y3+、Z2- D.X+、Z2-
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。下列说法正确的是( )

A.Y、W的最简单氢化物的水溶 液都呈酸性
液都呈酸性
B.X、Y与Z中的任意两种元素均可形成两种或两种以上的化合物
C.上述四种元素形成的化合物都抑制水的电离
D.W的单质可从Z的最简单氢化物中置换出Z的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。

请回答下列问题:
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是____________________________;
(2)图中ΔH=________kJ·mol-1;
(3)V2O5的催化循环机 理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:_____________________________________________;
理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式:_____________________________________________;
(4)已知单质硫的燃烧热为296 kJ·mol-1,计算由S(s)生成3 mol SO3(g)的ΔH(要求计算过程)。(已知燃烧热是指25 ℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量)
查看答案和解析>>
科目:高中化学 来源: 题型:
知:C(s)+H2O(g)=CO(g)+H2(g) △H=a kJ/mol
C(s)+O2(g)=2CO(g) △H=-220 kJ/mol
H-H、O=O和O-H键的键能分别为436、496和462 kJ/mol,则a为
A.-332 B.-118 C.+350 D.+130
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=== NH 4Cl(s)在室温下可自发进行,则该反应的△H<0
4Cl(s)在室温下可自发进行,则该反应的△H<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH 溶液加水稀释后,溶液中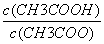 的值减小
的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
水是地球上最常见的物质之一,是包括人类在内所有生命生存的重要资源,也是生物体最重要的组成部分。有关水的反应有很多,依据题意回答下列问题。
(1)水分子自身电离出电子数相等的阴、阳两种离子,其中阳离子的化学式为________。
(2)常温下,某溶液中由 水电离的c(H+)=1×10-12mol·L-1,该溶液可能是________。
水电离的c(H+)=1×10-12mol·L-1,该溶液可能是________。
①二氧化硫水溶液 ②氯化铵水溶液 ③碳酸氢钠水溶液 ④氢氧化钠水溶液
(3)写出有水参与的氧化还原反应,但水既不是氧化剂也不是还原剂,写出离子方程式:______________________ _______________ _______________________
_______________ _______________________ _________(任写一个)。
_________(任写一个)。
(4)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-、NO 和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式:_____________ _______________________________________________________。
和CN-等有毒有害的还原性酸根离子氧化除去。请写出用ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式:_____________ _______________________________________________________。
(5)CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206kJ·mol-1;又知CH4(g)+2O2(g)===CO2(g)+2H2O(g)
ΔH=-802kJ·mol-1。试写出由CO2与H2O反应生成CO的热化学方程式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.合成氨工业中,移走NH3可增大正反应速率,提高原料转化率
B.酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液
C.将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深
D.牺牲阳极的阴极保护法和外加直流电的阴极保护法都是应用电解原理
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com