
如图所示三套实验装置,分别回答下列问题。
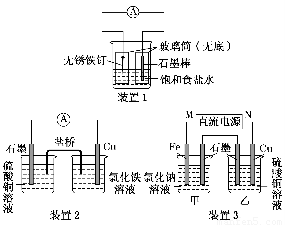
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀,表明铁被________(填“氧化”或“还原”); 向插入石墨棒的玻璃筒内滴入酚酞溶液,可观察到石墨棒附近的溶液变红,该电极反应式为________________________________________________________________________。
(2)装置2中的石墨是________极(填“正”或“负”),该装置发生的总反应的离子方程式为________________________________________________________________________。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________极;甲烧杯中铁电极的电极反应式为_________________。
②乙烧杯中电解反应的离子方程式为_________________________________。
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下的体积为________mL。
(1)氧化 O2+4e-+2H2O=4OH- (2)正 2Fe3++Cu=2Fe2++Cu2+
(3)①正 Fe-2e-=Fe2+ ②2Cu2++2H2O 2Cu+O2↑+4H+ ③224
2Cu+O2↑+4H+ ③224
【解析】(1)装置1,由石墨棒附近的溶液变红可知,石墨棒作正极,电极反应式为O2+4e-+2H2O=4OH-,铁钉作负极,发生氧化反应。
(2)由装置2两电极活泼性强弱得Cu一定是负极,总反应的离子方程式即该装置中自发的氧化还原反应:2Fe3++Cu=2Fe2++Cu2+。
(3)①由甲中石墨电极附近首先变红可知该极H+放电,即该极为阴极,Fe为阳极,电极反应式为Fe-2e-=Fe2+,由此可知,电源M端为正极;
②电源M端为正极,N端为负极,乙中Cu为阴极,石墨为阳极,发生反应的离子方程式为2Cu2++2H2O 2Cu+O2↑+4H+;
2Cu+O2↑+4H+;
③由两池中的对应关系Cu~2e-~H2↑
? 64 g? 1 mol
? 0.64 g? 0.01 mol
即224 mL H2。


科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程。
(1)甲、乙、丙三位同学均采取乙醇、冰醋酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是 ;
(2)甲、乙、丙三位同学分别设计了如图所示三套实验装置:
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是 (选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是 。
(3)试管②中饱和Na2CO3的作用除了溶解乙醇、降低乙酸乙酯溶解度外,还可以 。
(4)从试管②中分离出乙酸乙酯的实验操作是 。
(5)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反
应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源:2010—2011学年浙江省杭州师范大学附属中学高二上学期期末考试化学试卷 题型:实验题
(13分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程。
(1)甲、乙、丙三位同学均采取乙醇、冰醋酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是 ;
(2)甲、乙、丙三位同学分别设计了如图所示三套实验装置: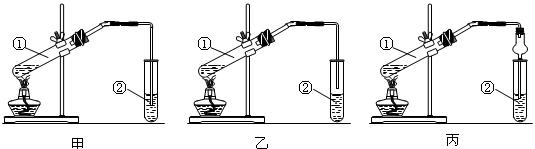 请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是 (选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是 。
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是 (选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是 。
(3)试管②中饱和Na2CO3的作用除了溶解乙醇、降低乙酸乙酯溶解度外,还可以 。
(4)从试管②中分离出乙酸乙酯的实验操作是 。
(5)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反
应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
科目:高中化学 来源:2012届浙江省高二上学期期末考试化学试卷 题型:实验题
(13分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程。
(1)甲、乙、丙三位同学均采取乙醇、冰醋酸与浓硫酸混合共热的方法制取乙酸乙酯,浓硫酸的作用是 ;
(2)甲、乙、丙三位同学分别设计了如图所示三套实验装置:
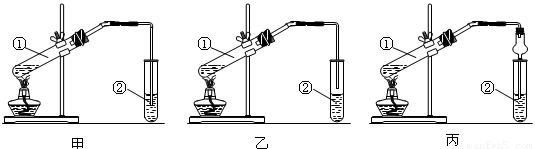 请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是
(选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是
。
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,应选择的装置是
(选填“甲”或“乙”)。丙同学设计了丙装置,用球形干燥管代替玻璃管,除了起到冷凝作用外,另一重要作用是
。
(3)试管②中饱和Na2CO3的作用除了溶解乙醇、降低乙酸乙酯溶解度外,还可以 。
(4)从试管②中分离出乙酸乙酯的实验操作是 。
(5)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,
就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反
应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com