
�����ߡ������־���ҹ��ĺ�����ҵ�������µ�ƪ�¡�
��1���������ʱ�������������ľ���Ħ�����������¡�Ϊ�˷�ֹ����¶ȹ��ߣ��ڻ��һ��Ϳ��һ�������Ϳ�ϣ���Ϳ�ϵ���������ܵ��� ��
| A���ڸ����²��ڻ� | B���ڸ����¿ɷֽ����� |
| C���ڳ����¾ͷֽ����� | D����Ϳ�ϲ����ܷ����ֽ� |

 CH4(g)+HC��CH(g)+H2(g)�� ��H1="156.6" kJ��mol-1
CH4(g)+HC��CH(g)+H2(g)�� ��H1="156.6" kJ��mol-1 CH4(g)+ HC��CH (g)����H2="32.4" kJ��mol-1
CH4(g)+ HC��CH (g)����H2="32.4" kJ��mol-1 CH3CH=CH2(g)+H2(g)�ġ�H=_____kJ��mol-1
CH3CH=CH2(g)+H2(g)�ġ�H=_____kJ��mol-1 ��1��B ��2��1 2 3 4 ��2��1 ��������Ⱦ��3��H2-2e-+2OH-=2H2O 2
��4��2CO2+4e-+2H2O=2CO+4OH- ������ ��H>0������ ��S<0 ��5��(124.2)
���������������Ϳ�ϵ���������ܵ����ڸ����¿ɷֽ��������ֽ����ȣ���������Ҳ���Ĵ���������������ʹ����¶Ƚ��͡�ѡ��Ϊ��B����2�����������Ҫ�������ܵķ�Ӧ�ķ���ʽ��1N2O4+2N2H4==3N2+4H2O��ϵ����1 2 3 4���÷�Ӧ�б�����N2H4�е�N��ԭ���뱻��ԭ��ԭ�ӵ�N2O4�е�Nԭ�ӵ����ʵ���֮����2:1. �����ӦӦ���ڻ���ƽ��������ͷŴ������ȺͿ��ٲ������������⣬����һ���ܴ���ŵ��Dz�������Ⱦ���ྻ����������3��������ȼ�ϵ���У�ͨ��H2�ĵ缫�������������ĵ缫��ӦΪ��H2-2e-+2OH-=2H2O. 2H2O------2H2��+ O2������������3mol,ת�Ƶ���4mol.���ڲ������干1.5mol������ת�Ƶ���2mol.��4�������ܷ�Ӧʽ�������ĵ缫��Ӧʽ�ɵõ�������ӦΪ:2CO2+4e-+2H2O=2CO+4OH- �������2CO=2C+O2����H��0����S��0��������CO����Ⱦ�ķ��������С�ԭ���Ǹ÷�Ӧ�ġ�H>0�������ȷ�Ӧ����S<0����ϵ�Ļ��ҳ̶ȼ�С����5����-�������ã�C3H8(g)  CH3CH=CH2(g)+H2(g)�ġ�H=124.2KJ/mol.
CH3CH=CH2(g)+H2(g)�ġ�H=124.2KJ/mol.
���㣺���麽����ҵ�漰���ĸ������⼰��ѧ��Ӧ�����������ȵ�֪ʶ��


 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д� ���Ž�����ٰθ��νӹ㶫���������ϵ�д�
���Ž�����ٰθ��νӹ㶫���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������(H2O2)��һ����ɫ��Һ��,����ˮ��Һ�׳�˫��ˮ,��������,����������������ɱ������Ư���ȡ�
(1)����˵����ȷ���� ��
| A��������������м��м��Լ����зǼ��Լ� |
| B��H2O2��H2O��Ϊͬ�������� |
| C��34 g H2O2�к��е���������ΪNA |
| D��ʵ���ҿ������ù���������ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���û��ϼۺ���������Ʋ����ʵ������ǻ�ѧ�о�����Ҫ�ֶΡ�
��1���ӻ��ϼ۵ĽǶȿ���Ԥ�����ʵ����ʡ�
��SO2������___________������ţ���ͬ����
A��ֻ�������� B��ֻ�л�ԭ�� C���������������л�ԭ��
�ڽ�SO2ͨ������KMnO4��Һ�У���Һ����ɫ������ɫ����Ӧ��������Ԫ�ش�����ʽ��������__________��
A��S2�� B��S C��SO32�� D��SO42��
��2�������ʷ���ĽǶȿ����Ʋ����ʵ����ʡ�������MgO��Al2O3��Fe2O3��SiO2��ɵ�ij�����������
������Al2O3����_______�����MgO��Fe2O3����_________���������ԡ��������ԡ������ԡ�����
�ڽ��������ڹ����������У����ˣ���������Ҫ�ɷ���_________��������Һ�м���NaOH��Һ�����������ˣ������е���Ҫ�ɷ���_________��
������������ֱ�����ڹ�����NaOH��Һ�У��������ķ�Ӧ�Ļ�ѧ����ʽ��______________________��������д����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����������Ļ������ڹ�����ռ����Ҫ��λ���ϳɰ���ҵ�У��ϳ�����ÿ����2 mol NH3���ų�92.4 kJ������
��1������ʼʱ�������ڷ���2 mol N2��6 mol H2����ƽ���ų�������ΪQ����Q_____184.8kJ���>������<����=���� �� һ�������£����ܱպ��ݵ������У��ܱ�ʾ��Ӧ�ﵽ��ѧƽ��״̬����____________��
a��3v��(N2)=v��(H2) ������ b��2v��(H2)= v��(NH3)
c����������ܶȱ��ֲ��� �� d��c(N2)��c(H2)��c(NH3)=1��3��2
��ҵ�������ص�ԭ������NH3��CO2Ϊԭ�Ϻϳ�����[CO(NH2)2]����Ӧ�Ļ�ѧ����ʽΪ2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l)��
CO(NH2)2 (l) + H2O (l)��
��2����һ���¶Ⱥ�ѹǿ�£���ԭ�����е�NH3��CO2�����ʵ���֮�ȣ���̼�ȣ�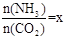 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ����___________��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ����___________��
��3��ͼ�е�B�㴦��NH3��ƽ��ת����Ϊ_______��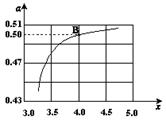
��֪��3Cl2+2NH3��N2+6HCl �D�D�� 3Cl2+8NH3��N2+6NH4Cl �D�D��
��4����ɲ���ƽ����������ԭ��Ӧ����ʽ���ٱ������ת�Ƶķ������Ŀ��
12Cl2+15NH3�� �D�D��
��5����Ӧ���еĻ�ԭ���� ����ԭ������ ��
��6�������۷�Ӧ���������9.408L����״����������������������ʵ����� mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���Ṥ���������к���SO2���ж��ַ�����ʵ����������
��1����ҵ������Ĺ����У�SO2�����������Ļ�ѧ����ʽΪ ��
��2����ʪʽ���շ����������ռ���SO2������Ӧ�Ӷ�����
��֪��25��ʱ��H2SO3  HSO3 -+H+ K=1.5��10-2
HSO3 -+H+ K=1.5��10-2
H2CO3 HCO3 -+H+ K=4.4��10-7
HCO3 -+H+ K=4.4��10-7
�����Լ����ʺ������÷����ռ����� ������ĸ��ţ���
a.ʯ���� b. Na2SO3��Һ c. Na2CO3��Һ
�ڡ��Ƽ����NaOH��Һ�����ռ�����100 mL 0.2 mol��L-1��NaOH��Һ��ͨ���״����0.448 L SO2���壬��Ӧ������ҺpH<7������Һ�����и�����Ũ�ȹ�ϵ��ȷ���� ������ĸ��ţ���
a.c(HSO3-)> c(SO32-)> c(H2SO3)
b.c(Na+)>c(HSO3-)> c(H+)> c(SO32-)
c.c(Na+)+c(H+)= c(HSO3-)+c(SO32-)+c(OH-)
��3��ij���᳧��������������Cr2O72-�����Է�ˮ���������ͬʱ�Ʊ�Cr2O3��Ʒ�������������£�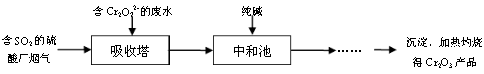
���������з�Ӧ��ĸ�Ԫ����Cr3+��ʽ���ڣ������з�����Ӧ�����ӷ���ʽΪ ��
���кͳ��еķ�Ӧ������Cr(OH)3�����⣬�������ij�����壬������Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
I��1���ڵ��۵⻯����Һ��ͨ�����������������ῴ����Һ����ɫ����Ӧ�����ӷ���ʽ�� ��
��2���ڵ�͵����γɵ���ɫ��Һ��ͨ��SO2���壬������ɫ����ʧ����Ӧ�����ӷ����� ��
��3���Աȣ�1���ͣ�2��ʵ�����õĽ������Cl ��I
��I SO2����ԭ����ǿ����˳������Ϊ ��
SO2����ԭ����ǿ����˳������Ϊ ��
II ��4�� ��ȥ�����л������۵��Լ��� �����ӷ���ʽΪ
��5�� 1mol����������2mol̼�����ƹ����Ϻ����ܱ������м��ȳ�ַ�Ӧ���ų��������ʺ���ȴ�������Ĺ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ������ͼ��ʾ����������ˮ�μӻ����ɵļ��ַ�Ӧ��
��CaO+H2O =Ca(OH)2
��2Na+H2O=2NaOH+H2��
��H2+CuO  Cu +H2O
Cu +H2O
��3S+6NaOH  2Na2S +Na2SO3 +3H2O
2Na2S +Na2SO3 +3H2O
��NaOH+HCl=NaCl+H2O
��ش��������⣺
��1����Ӧ����ˮ ������ĸ����
| A���������� |
| B���ǻ�ԭ�� |
| C���������������ǻ�ԭ�� |
| D���Ȳ����������ֲ��ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ���ů��ʹ�ö���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Եø��ӽ��ȡ������û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯��������ʡ�
��1�����������ҹ���������̼���о�ȡ���ش��չ���õ绡���ϳɵ�̼�����г����д���̼�����������ʣ�������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��
__C+__K2Cr2O7+__ ��__CO2��+ __K2SO4 + __Cr2(SO4)3+__H2O
����ɲ���ƽ������ѧ����ʽ��
��2���״���һ������ȼ�ϣ��״�ȼ�ϵ�ؼ�����ʵ��������ҵ����������ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��CO��g��+ 2H2��g�� CH3OH��g�� ��H1����116 kJ��mol-1
CH3OH��g�� ��H1����116 kJ��mol-1
�����д�ʩ������������÷�Ӧ�ķ�Ӧ���ʵ��� _______��
| A����ʱ��CH3OH�뷴Ӧ�������� | B�����ͷ�Ӧ�¶� |
| C��������ϵѹǿ | D��ʹ�ø�Ч���� |
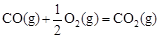 ��H2����283 kJ��mol-1
��H2����283 kJ��mol-1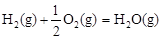 ��H3����242 kJ��mol-1
��H3����242 kJ��mol-1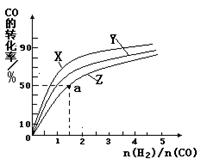
 CH3OH��g����ƽ�ⳣ��K = ��
CH3OH��g����ƽ�ⳣ��K = ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������ԭ��Ӧ�����ǻ�ѧѧ�Ƶ���Ҫ����֮һ����Ҫ��ش��������⣺
(1) ����Ϊ���ܻ�ԭ����NaBH4����ˮ����ˮ��Ӧ��NaBH4+2H2O��NaBO2+4H2�����˷�Ӧ��BԪ�صĻ��ϼ�û�з����仯����NaBH4��H�Ļ��ϼ�Ϊ___________���÷�Ӧ����������______________����ԭ������______________��
(2) ������������Ӧ��
��Cl2+FeI2��FeCl2+I2 ����2Fe2++Br2��2Fe3++2Br������Co2O3+6HCl��2CoCl2+Cl2��+3H2O
�ٸ������Ϸ���ʽ���Եõ�Fe2+��Co2+��Br����I����ԭ����ǿ������˳��Ϊ_________��
��1molCo2O3������HCl�����ʵ���_____________��
(3) ��ɲ���ƽ���л�ѧ��Ӧ����ʽ��
��KMnO4+��H2C2O4+��________ ��CO2+��K2SO4+��MnSO4+��H2O
��CO2+��K2SO4+��MnSO4+��H2O
(4)һ��������������ԭ��Ӧ����ʽ���Բ�д���������뷴Ӧʽ����һ���ǡ�������Ӧʽ����һ���ǡ���ԭ��Ӧʽ������2H+ +Zn��Zn2++H2�����ɲ�дΪ������Ӧʽ��Zn��2e����Zn 2+����ԭ��Ӧʽ��2H++ 2e����H2�������ɴ�ʵ���˻�ѧ������ܵ��ת�����ݴˣ��ش��������⣺
�ٽ�2Fe3++Cu= 2Fe2+ +Cu2+��дΪ�������뷴Ӧʽ�������У�������ӦʽΪ ��
���ɢ��еķ�Ӧ������Ƴ�����ͼ��ʾ��ԭ��أ�
���缫aΪCu ���������Һ�Ļ�ѧʽΪ ��
�缫b���ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com