

| A. | 步骤①的操作名称是溶解 | |
| B. | 步骤②中玻璃棒的作用是引流 | |
| C. | 步骤③的操作名称是蒸发 | |
| D. | 步骤④中的双氧水加入滤渣后迅速产生大量气泡 |
分析 溶解时用玻璃棒搅拌的主要目的是加速其中的电解质溶解于水;废干电池中的氯化铵和氯化锌可溶于水;灼烧的目的是除去滤渣中的炭黑和淀粉等,二氧化锰能催化过氧化氢分解放出氧气,从而间接检验二氧化锰,
A、装置图分析可知①是在烧杯中用水溶解废干电池筒中固体;
B、②是过滤装置,用来分离固体和液体;
C、③为坩埚中灼烧固体的装置,利用酒精灯加热,玻璃棒搅拌,在泥三角上加热坩埚,搅拌防止局部受热固体飞溅;
D、④为灼烧后的滤渣和过氧化氢混合其中二氧化锰催化剂使过氧化氢分解生成氧气.
解答 解:A、装置图分析可知①是在烧杯中用水溶解废干电池筒中固体,步骤①的操作名称是溶解,故A正确;
B、②是过滤装置,用来分离固体和液体,名称为过滤,步骤②中玻璃棒的作用是引流,故B正确;
C、③为坩埚中灼烧固体的装置,利用酒精灯加热,玻璃棒搅拌,在泥三角上加热坩埚,步骤③的操作名称是灼烧,蒸发应在蒸发皿中进行,故C错误;
D、灼烧后的滤渣和过氧化氢混合其中二氧化锰催化剂使过氧化氢分解生成氧气,2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,步骤④中的双氧水加入滤渣后迅速产生大量气泡,故D正确;
故选C.
点评 本题考查了化学实验基本操作的理解应用,物质分离的方法和步骤,主要是仪器使用,操作过程,物质成分的分析判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.03 mol/(L•s) | ||
| C. | v(B)=0.90 mol/(L•min) | D. | v(C)=0.60 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
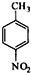
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 和 CH3CH2CH2CH3⑤
和 CH3CH2CH2CH3⑤ 和
和
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑤⑥⑦ | B. | ②③④⑤ | C. | ①②④⑤⑥⑦ | D. | ①②③④⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com