
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  △H3
△H3
回答下列问题:
化学键 | H-H | C-O | C | H-O | C-H |
E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H1= kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3= kJ.mol-1
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是  。
。
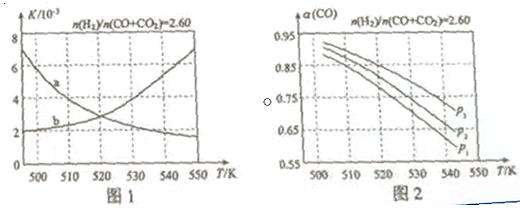
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而 (填“增大”或“减小”),其原因是 。图2中的压强由大到小为_____,其判断理由是_____。
【答案】(1)—99;+41 (2)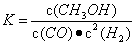 ;a;反应①为放热反应,平衡常数应随温度升高变
;a;反应①为放热反应,平衡常数应随温度升高变
小;
(3)减小;升高温度时,反应①为放热反应,平衡向向左移动,使得体系中CO的量增大;反应③为吸热反应,平衡向右移动,又产生CO的量增大;总结果,随温度升高,使CO的转化率降低;P3>P2>P1;相同温度下,由于反应①为气体分子数减小的反应,加压有利于提升CO的转化率;而反应③为气体分子数不变的反应,产生CO的量不受压强影响,故增大压强时,有利于CO的转化率升高
 的量不受压强影响,故增大压强时,有利于CO的转化率升高,所以图2中的压强由大到小为P3>P2>P1。
的量不受压强影响,故增大压强时,有利于CO的转化率升高,所以图2中的压强由大到小为P3>P2>P1。
考点:考查反应热计算、盖斯定律应用以及外界条件对平衡状态的影响


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)=2HCl(g),ΔH = —184.6 kJ·mol-1
则反应HCl(g)= 1/2H2(g)+1/2Cl2(g)的ΔH是
A.+184.6kJ·mol-1 B.—369.2 kJ·mol-1
C.+92.3 kJ·mol-1 D.—92.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是 。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3 氧化酸性FeCl2 废液得到FeCl3 。
①若酸性FeCl2 废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3 氧化FeCl2 的离子方程式:
| |
 ClO3-+
ClO3-+ | |
 Fe2++
Fe2++ | |
 =
= | |
 Cl-+
Cl-+ | |
 Fe3++
Fe3++ | |
 .
. (3)FeCl3 在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
 欲使平衡正向移动可采用的方法是(填序号) 。
欲使平衡正向移动可采用的方法是(填序号) 。
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
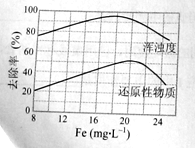
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约
为 mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上,向500—600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。
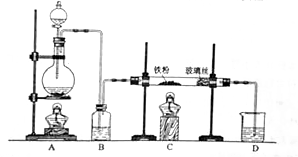
回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 ,装置B中加入的试剂是 。
(2)制取无水氯化亚铁的实验中,装置A用来制取 。尾气的成分是 。若仍用D的装置进行尾气处理,存在的问题是 、 。
(3)若操作不当,制得的FeCl2 会含有少量FeCl3 ,检验FeCl3常用的试剂是 。欲制得纯净的FeCl2 ,在实验操作中应先 ,再 。
选考题(请考生在第18.19.20三题中任选一题作答,如果多做,则按所做的第一题计分.)
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德 罗常数的值。下列叙述正确的是
罗常数的值。下列叙述正确的是
A.60g丙醇中存在的共价键总数为10NA
B.1L 0.1mol·L-1的NaHCO3-溶液中HCO3-和CO32-离子数之和为0.1NA
C.钠在空气中燃烧可生成多种氧化物。23g钠充分燃烧时转移电子数为1NA
D.235g核互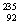 U发生裂变反应:
U发生裂变反应: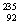 U+
U+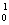 n
n
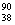 Sr+
Sr+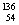 U+10
U+10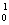 n净产生的中子(
n净产生的中子(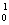 n)数为10NA
n)数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
正误判断,正确的划“√”,错误的划“×”
(1)在标准状况下,1 mol O2与1 mol SO3的体积相同( )
(2)在标准状况下,1 mol气体的体积约是22.4 L,在非标准状况下,1 mol气体的体积则一定不是22.4 L( )
(3)22.4 L气体在标准状况下是1 mol,在非标准状况下一定不是1 mol( )
(4)在相同条件下,相同物质的量的CO、N2的混合气体与O2的分子个数相同,原子个数也相同( )
(5)在相同条件下,相同物质的量的C2H4和C3H6,所含分子个数相同,原子个数也相同( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于同温同压下的两种气体12C18O和14N2的判断正确的是 ( )
A.体积相等时密度相等
B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等
D.质量相等时具有的质子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
100℃时水的离子积约为1.0×10-12,则此时纯水中C(H+)= ,
PH= ,溶液呈 性;此温度下,0.05mol/L的硫酸的PH= ,0.1mol/L的氢氧化钠溶液的PH=
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com