

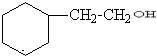 .
. .
.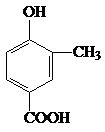 +CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O.分析 (1)A中含-酚-OH、-COOH;
(2)B与足量氢气充分反应时,苯环和醛基都能发生加成反应;
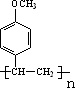
(3)D中含碳碳双键,可发生聚合反应;
(4)A中含-COOH,与乙醇发生酯化反应;
(5)a.B、D与Na不反应;
b.C、D中均含碳碳双键;
c.C不与碳酸氢钠反应;
d.酚-OH的邻、对位与溴发生取代反应,碳碳双键与溴发生加成反应.
解答 解:(1)A中含-官能团的名称为羟基、羧基,故答案为:羟基、羧基;
(2)B与足量氢气充分反应时,苯环和醛基都能发生加成反应,其产物结构简式为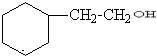 ,故答案为:
,故答案为: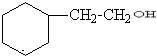 ;
;
(3)D中含碳碳双键,可发生聚合反应,则聚合产物的结构简式为 ,故答案为:
,故答案为: ;
;
(4)A中含-COOH,与乙醇发生酯化反应,该反应为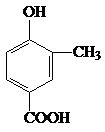
 +H2O,
+H2O,
故答案为: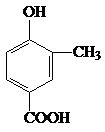
 +H2O;
+H2O;
(5)a.B、D与Na不反应,含-OH、-COOH与Na反应,故a错误;
b.C、D中均含碳碳双键,则C、D均能使溴的四氯化碳溶液褪色,故b正确;
c.C不含-COOH,则C不与碳酸氢钠反应,故c错误;
d.酚-OH的邻、对位与溴发生取代反应,碳碳双键与溴发生加成反应,则1molC最多能与4molBr2发生反应,故d正确;
故答案为:bd.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意酚、醛、羧酸、烯烃等有机物的性质,题目难度不大.


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙醇不能发生氧化反应 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 由乙酸和乙醇制乙酸乙酯与由苯制取硝基苯反应属于同一类型的反应 | |
| D. | 苯和乙烷都能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时应使混合物中的水分完全蒸干后,才能停止加热 | |
| B. | 过滤时,将待过滤的物质沿玻璃棒倒入过滤器时,玻璃棒下端应靠在三层滤纸处 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一个烧杯中 | |
| D. | 蒸馏操作时,温度计应插入在溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
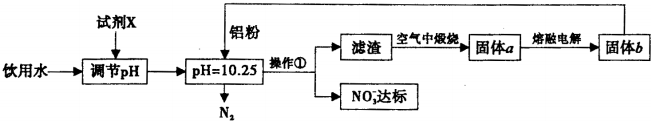
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将钠块投入到硫酸铜溶液中,可析出单质铜 | |
| B. | 将钠块长时间暴露在空气中的最终产物是Na2CO3 | |
| C. | Na2O与Na2O2阴阳离子个数比相同 | |
| D. | Na2O2能使品红溶液褪色且原理与SO2相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com