
| A.将足量的Na2O2和Na2O分别加入酚酞试液中,最终溶液均为红色 |
| B.用钠与空气反应制纯净的Na2O2,空气必须经过碱石灰处理后,才能与钠反应 |
| C.钠与钠离子都具有强还原性 |
| D.在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2 |
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.Na2CO3的稳定性介于Na2CO3·10H2O和NaHCO3之间 |
| B.“侯氏制碱法”制得的碱是指NaHCO3 |
| C.可用盐酸鉴别Na2CO3和NaHCO3固体 |
| D.纯碱有时可代替烧碱使用,比如溶解石英、吸收氯气等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁铝合金的熔点低于铝的熔点 |
| B.把稀H2SO4加入NaAlO2溶液中生成白色沉淀然后沉淀又溶解 |
| C.NaOH溶液不能长时间在分液漏斗中放置 |
| D.蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

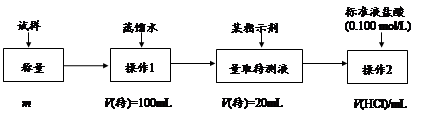
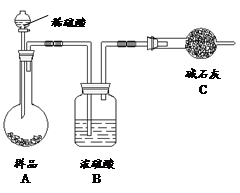
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等质量的Na2CO3、NaHCO3分别与足量稀盐酸反应,NaHCO3产生的CO2多 |
| B.等质量的Na2CO3、NaHCO3分别与足量的同种盐酸反应,NaHCO3消耗的盐酸多 |
| C.向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| D.Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.均为0.84 L | B.均为0.56 L |
| C.①>② | D.②>① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
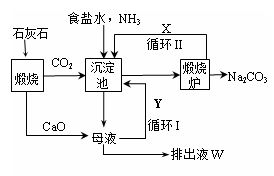
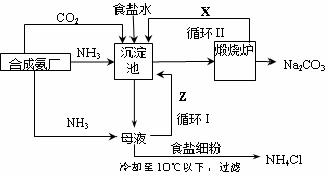
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
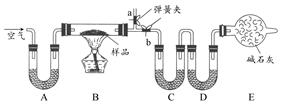
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Na>Al |
| B.若把铝钠合金投入一定量的水中只得到无色溶液,则n(Al)≤n(Na) |
| C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小 |
| D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com