
【题目】下图是教材中实验装置。

回答下列问题:
(1)甲仪器的名称是______,与同类仪器相比其优点是______、______。
(2)向乙通水,进水口是_______(填“a”或“b”),理由是_____________________。
(3)利用上述装置进行醇与酸的酯化反应。
①醇、酸、酯和水之间的沸点满足的条件是___________。
②如果外接一个装置可以满足蒸馏的条件,那么,此时醇、酸、酯和水之间的沸点满足的条件是____________________。
【答案】 分液漏斗 可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入 避免甲中液体散入到空气中 a 有利于向上排出空气,使水充满球形冷凝管 酯的沸点高于其他物质,且有机物易挥发 酯的沸点最低或者水的沸点最高
【解析】试题分析:(1)甲仪器的名称恒压分液漏斗,与同类仪器相比其优点是可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入;避免甲中液体散入到空气中。
(2)向乙通水,冷凝水低进高出有利于向上排出空气,使水充满球形冷凝管。
(3)利用上述装置进行醇与酸的酯化反应。①为了不让酯挥发,醇、酸、酯和水之间的沸点满足的条件是酯的沸点高于其他物质,且有机物易挥发,。
②如果外接一个装置,为让酯挥发出来,此时醇、酸、酯和水之间的沸点满足的条件是酯的沸点最低或者水的沸点最高。
解析:(1)根据图示,甲仪器的名称分液漏斗,与同类仪器相比其优点是可以保持三颈烧瓶与分液漏斗的压强相等,利于液体滴入;避免甲中液体散入到空气中。
(2)向乙通水,冷凝水低进高出有利于向上排出空气,使水充满球形冷凝管,向乙通水,进水口是a。
(3)①利用上述装置进行醇与酸的酯化反应,为了不让酯挥发,醇、酸、酯和水之间的沸点满足的条件是酯的沸点高于其他物质,且有机物易挥发。
②利用上述装置进行醇与酸的酯化反应,如果外接一个装置,为让酯挥发出来,此时醇、酸、酯和水之间的沸点满足的条件是酯的沸点最低或者水的沸点最高。


科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅱ]丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+![]() O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
O2(g)= C4H8(g)+H2O(g) ΔH2=119 kJ·mol1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=242 kJ·mol1
O2(g)= H2O(g) ΔH3=242 kJ·mol1
反应①的ΔH1为________kJ·mol1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是_________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
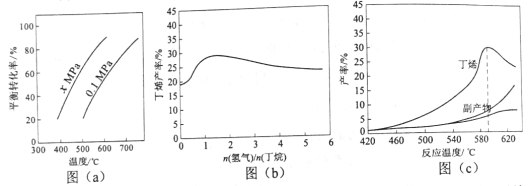
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是__________________________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠和铝均是重要的金属。
(1) 铝的原子结构示意图是___________________。
(2) 铝与NaOH溶液反应的离子方程式为______________________________;
(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为______________。
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2molNH3,下列对这四种气体的关系从大到小表达错误的是
A. 体积②>③>①>④ B. 密度②>③>④>①
C. 质量②>③>④>① D. 氢原子个数①>③>④>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置制取NH3,并用AlCl3溶液吸收多余NH3制Al(OH)3,最后回收NH4Cl,能达到实验目的的是

A. 用装置甲制取NH3
B. 用装置乙吸收NH3制取Al(OH)3
C. 用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌
D. 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工业合成氨反应 N2(g)+3H2(g) ![]() 2NH3 (g),以下分析不正确的是
2NH3 (g),以下分析不正确的是
A. 在5L固定容积的密闭容器内,前2分钟消耗2molN2,则v(N2)=0.2mol·L-1·min-1
B. 改变条件可使H2的转化率达100%
C. 每消耗3molH2,必然生成2molNH3
D. 合成氨是人类科学史上的一项重大突破,缓解了粮食不足问题
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1 mol·L-1。如果在甲瓶中加入少量的NaHCO3晶体(m mol),在乙瓶中加入少量的NaHSO3晶体(m mol),丙瓶不变。片刻后,甲、乙、丙三瓶溶液中HClO的物质的量浓度的大小关系是(溶液体积变化忽略不计( )
A.甲=乙>丙B.甲>丙>乙C.丙>甲=乙D.乙>丙>甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com