
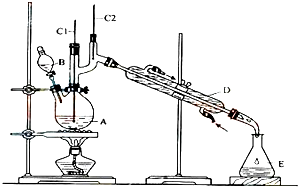
 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
分析 ①将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中,该物质作催化剂,注意先后顺序,相当于稀释浓硫酸;
②在A中加入4.0g正丁醇和几粒沸石,沸石防暴沸,加热;当有蒸汽出现时,开始滴加B中溶液,滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分,得到的馏分中含有正丁醛;
③将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g,得到正丁醛;
(1)不能将Na2Cr2O7溶液加到浓硫酸中,因为浓硫酸的密度大,容易发生迸溅;
(2)加入沸石的作用是防止暴沸,若加热后发现未加沸石,停止加热,冷却后补加;
(3)B仪器的名称是分液漏斗,D仪器的名称直形冷凝管;
(4)分液漏斗使用前必须检漏;
(5)由表中数据可知,正丁醛密度小于水的密度,据此判断;
(6)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90~95℃,既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化;
(7)设正丁醛的产率为x,则正丁醇的利用率为x,根据关系式C4H10O~C4H8O列方程计算.
解答 解:(1)因为浓硫酸的密度大,将Na2Cr2O7溶液加到浓硫酸中,容易发生迸溅伤人,不能将Na2Cr2O7溶液加到浓硫酸中,
故答案为:不能;浓H2SO4遇水放出大量的热,容易溅出伤人;
(2)加入沸石的作用是防止暴沸,若加热后发现未加沸石,应采取的正确方法是:停止加热,冷却后补加,
故答案为:防止暴沸;停止加热,冷却后补加;
(3)B仪器的名称是分液漏斗,D仪器的名称直形冷凝管,
故答案为:分液漏斗;直形冷凝管;
(4)B为分液漏斗使用前必须检漏,故选C,
故答案为:C;
(5)正丁醛密度为0.8017 g•cm-3,小于水的密度,故分层水层在下方,正丁醛置于分液漏斗中在上层,
故答案为:上;
(6)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90~95℃,既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化,为更好的控制温度,可以采取的改进措施是水浴加热,
故答案为:保证正丁醛及时蒸出,又可尽量避免其被进一步氧化; 水浴加热;
(7)设正丁醛的产率为x,则正丁醇的利用率为x,根据关系式,
C4H10O~C4H8O
74 72
4xg 2g
解得:x=$\frac{74×2}{72×4}$=51.4%,
故答案为:51.4.
点评 本题考查有机化学实验、反应原理、基本操作、化学计算等,题目难度不大,注意计算中正丁醇的转化率等于正丁醛的产率,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥⑧ | B. | ①④⑥⑧ | C. | ①④⑤⑥⑦ | D. | ②⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
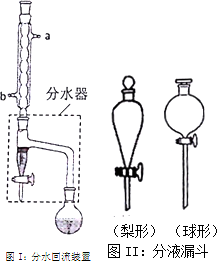 实验室制备乙酸正丁酯的化学方程式:
实验室制备乙酸正丁酯的化学方程式:| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度(g•cm-3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点(℃) | 118.0 | 118.1 | 126.1 | 142 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
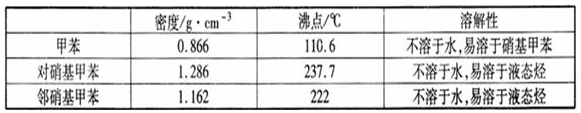
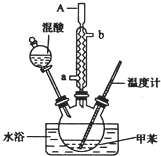 一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯).反应原理:
一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯).反应原理:
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=-0.33 kJ/mol | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3<0,单斜硫比正交硫稳定 | |
| D. | △H3>0,单斜硫比正交硫稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com