
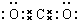 ��
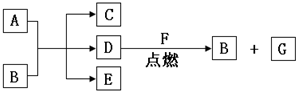
������ ��֪�������ʾ�Ϊ��ѧ��ѧ�г������ʣ�������A��ʹ�������ۻ�����AΪŨ�����Ũ���E��һ����ʹƷ����Һ��ɫ����ɫ���壬��EΪSO2��AΪŨ���B�ǹ���ǽ������ʣ�CΪˮ����BΪC��DΪCO2��D��F��ȼ����B��G����FΪ�������ʣ�G�������ͻ���ϣ���FΪMg��GΪMgO��BΪC���ݴ˽��н��
��� �⣺������A��ʹ�������ۻ�����AΪŨ�����Ũ���E��һ����ʹƷ����Һ��ɫ����ɫ���壬��EΪSO2��AΪŨ���B�ǹ���ǽ������ʣ�CΪˮ����BΪC��DΪCO2��D��F��ȼ����B��G����FΪ�������ʣ�G�������ͻ���ϣ���FΪMg��GΪMgO��BΪC��
��1��DΪCO2��������̼Ϊ���ۻ���������ʽΪ��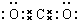 ��
��
�ʴ�Ϊ��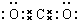 ��
��
��2��DΪCO2��FΪMg��GΪMgO��BΪC��D+F��B+G�Ļ�ѧ����ʽΪ��CO2+2Mg$\frac{\underline{\;��ȼ\;}}{\;}$ C+2MgO��
�ʴ�Ϊ��CO2+2Mg$\frac{\underline{\;��ȼ\;}}{\;}$ C+2MgO��
��3��A��ϡ��ҺΪϡ���ᣬ��Һ��������Ϊ��������ӣ�������������ӵķ���Ϊ���ȼ������ᣬ�������ټ����Ȼ�����Һ��������ɫ������
�ʴ�Ϊ���ȼ������ᣬ�������ټ����Ȼ�����Һ��������ɫ������
���� ���⿼�������ƶϣ���Ŀ�Ѷ��еȣ����ʵ����ʼ�ת�������ⷴӦΪ�ƶ�ͻ�ƿڣ�ע��Mg�������̼�ķ�Ӧ����������Ԫ�ػ��������ʣ�����������ѧ���ķ������������Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ����ֻ����Cu��Fe��Mg�Ͳ�ͬŨ�ȵ����ᣨ0.5mol/L��2mol/L��18.4mol/L�������ʵ�鷽�����о�Ӱ�췴Ӧ���ʵ����أ���ͬѧ�о���ʵ�鱨�������
����ֻ����Cu��Fe��Mg�Ͳ�ͬŨ�ȵ����ᣨ0.5mol/L��2mol/L��18.4mol/L�������ʵ�鷽�����о�Ӱ�췴Ӧ���ʵ����أ���ͬѧ�о���ʵ�鱨�������| ʵ �� �� �� | �� �� | �� �� |
| �ٷֱ�ȡ�������2mol/L�������Թ��У� �ڷֱ�Ͷ���С����״��ͬ��Cu��Fe��Mg�� | ��Ӧ������ Mg��Fe��Cu | ��Ӧ�������Խ���ã���Ӧ����Խ�죮 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1����2�� | B�� | ��2����3�� | C�� | ��3����4�� | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ԫ������Ȼ���ж����Ի���̬�����ں�ˮ�������� | |
| B�� | ͨ������£��������е����ԡ������ԡ�����չ�� | |
| C�� | �������˳�����������ǰ�Ľ����������ᷴӦ�û������е��� | |
| D�� | �Ͻ��Ӳ�ȣ��۵�һ�����ɽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 2��3 | C�� | 3��2 | D�� | 35��56 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �²��ϰ����������ǽ������Ϻ����л��߷��Ӳ��� | |
| B�� | �������ά�IJ����ǵ����� | |
| C�� | ��������ʵ�����Ʊ��������ڶ�������ṹ�Ķ�����̼ԭ�Ӿ�����ɱ�����ͬ���칹�� | |
| D�� | �л��߷��Ӳ���ȫ����ͨ���Ӿ۷�Ӧ�����۷�Ӧ�ϳɵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com