
����Ŀ��I�����п����ڷ�����ᴿ���ʵķ�����
��1����ȥCaO�л��е�CaCO3����____
��2������CCl4��ˮ�Ļ����_____
��3��������ˮ�е����ˮ______
��4����ȥ����ʯ��ˮ��������CaCO3����______
II���������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�á�

��1��д���������������ƣ���_____________��______________
��2��������װ��I�������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ�����____________������I�������ʱ��ˮ��Ϊ______����f��g����
��3����������500mL 0.2 mol/L NaOH��Һ������װ��II�Ǹ�ͬѧת����Һ��ʾ��ͼ����ͬѧ�����Ĵ����� _______________��_____________________��
���𰸡����� ��Һ ��ȡ ���� ������ƿ 1000mL����ƿ �¶ȼ� g δ�ò��������� ����ƿ���ѡ�����
��������
I����1��̼��Ʋ��ȶ�,���ȿɷֽ����������ƺͶ�����̼,���ü��ȵķ�������,���Ǽ�����
��2��ˮ��CCl4�Ļ����ֲ�,���÷�Һ�ķ�������,��˴��Ƿ�Һ��
��3��������ˮ�е����ˮ���������л��ܼ��������Ȼ�̼�����Բ�����ȡ�ķ������룬��˴�����ȡ��
��4��̼��Ʋ�����ˮ,���ù��˵ķ�������,��ˣ����ǹ���;
II����1��������ƿ����1000mL����ƿ��
��2��������װ��I�������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ������¶ȼƣ�����I�������ʱ��ˮ��Ϊg��
��3����������500mL 0.2 mol/L NaOH��Һ������װ��II�Ǹ�ͬѧת����Һ��ʾ��ͼ����ͬѧ�����Ĵ�����δ�ò���������������ƿ���Ӧѡ��500mL���𰸣�δ�ò���������������ƿ���ѡ�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ɸ�������ɺ����ʽ��з��ࡣ
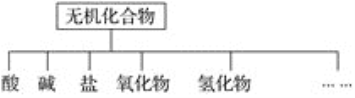
��1����ͼ��ʾ�����ʷ����������________��
��2����Na��K��H��O��C��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±�����
___________��______________��_______________
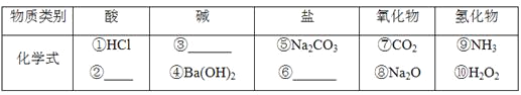
��3��д����ת��Ϊ�ݵĻ�ѧ����ʽ��__________________________________________��
��4��ʵ�����Ʊ��߳���________��________��Ӧ�����������ķ�����_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ�ɷ�Ϊһ����Դ�Ͷ�����Դ,��Ȼ�������ֳ���ʽ�ṩ����Դ��Ϊһ����Դ,������������Դ�����������ȡ����Դ��Ϊ������Դ���ݴ��ж�,����������ȷ����
A. ��Ȼ���Ƕ�����Դ B. ʯ���Ƕ�����Դ
C. ������һ����Դ D. ˮ����һ����Դ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶���,1L�����ܱ������з�����Ӧ:2A(g)+B(g)![]() C(g) ��H��������������,�ı���ʼA��B��Ͷ�ϱȵõ���ͼ��ʾ��ϵ������˵���������
C(g) ��H��������������,�ı���ʼA��B��Ͷ�ϱȵõ���ͼ��ʾ��ϵ������˵���������
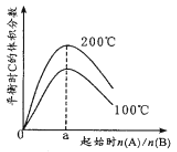
A. n(A)/n(B)=2ʱ��A��B��ת������� B. ��H<0
C. a=2 D. ��ͬ�¶��£�ƽ�ⳣ������ʼͶ�ϱ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ������������ԭ��Ӧ����
A. 2NaOH��H2SO4===Na2SO4��2H2O B. 3CO��Fe2O3![]() 3CO2��2Fe
3CO2��2Fe
C. 2Na+2H2O====2NaOH+H2�� D. 2Na2O2��2CO2===2Na2CO3��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�Ϊ10 L���ܱ������г���1mol H2��1mol I2,����һ���¶���ʹ�䷢����Ӧ:H2(g)+I2(g) ![]() 2HI(g)��20min��ﵽƽ��,���c(HI)=0.04 mol/L��
2HI(g)��20min��ﵽƽ��,���c(HI)=0.04 mol/L��
(1)��Ӧ�ӿ�ʼ��ƽ��ʱ��v(H2)Ϊ_______,ƽ�ⳣ��K=__________��
(2)�¶Ȳ��䣬�ﵽƽ������������ٳ���1molHI����,ƽ����________ (������������ƶ���)�ƶ�;�ٴ�ƽ���,HI�����������________ (���������С�����䡱)
(3)��(2)����ƽ����ϵ����,ƽ���I2���������Ϊ45%,�����º�H2��ת���ʽ�_____(���������С���� �䡱)���÷�Ӧ�Ħ�H_____0(�>������ <����=��)��
(4)���(3)�뻭��2HI(g)![]() H2(g)+I2(g)��ƽ�ⳣ��K���¶ȱ仯������ͼ��
H2(g)+I2(g)��ƽ�ⳣ��K���¶ȱ仯������ͼ��
 _____
_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���÷�������(��Ҫ�ɷ�ΪNiO��Al,����Cr��Fe��C��S���л���)�Ʊ�Ni(NO3)2��6H2O��ʵ���������£�
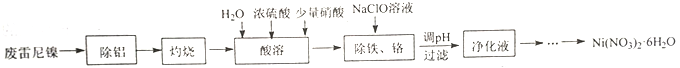
��֪������ʵ�������£�Ni2+��Cr3+����Һ�в��ܱ�NaClO��HNO3������
��NiSO4������ˮ��NiCO3������ˮ;Ni(NO3)2��20�桢90��ʱ�ܽ������Ϊ79.2��188g/100gˮ��
�ۼ�֪�������������Һ����Ҫ���������ӿ�ʼ�����������ȫ��pH���£�
Ni2+ | Fe2+ | Fe3+ | Cr3+ | |
��ʼ����pH | 6.2 | 7.6 | 2.3 | 4.5 |
������ȫpH | 8.5 | 9.1 | 3.3 | 5.6 |
��1���������������Լ�����Ҫ����Ϊ__________��
��2��������������ҪĿ����__________��
��3����������ʱ����Ũ�����ˮ����ϡ�����Ŀ����__________��
��4��������������ʱ��Fe2+������ΪFe3+�����ӷ���ʽΪ__________���������轫��ҺpH�������ķ�Χ��__________��
��5���������������Һ����ȡNi(NO3)2��6H2O��ʵ�鷽����__________�����ķ��롢ϴ�ӡ������Ni(NO3)2��6H2O (ʵ������ʹ�õ��Լ��У�6mol��L-1���ᣬ3 mol��L-1Na2CO3��Һ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A. Fe-Cu-CuSO4��Һ��ɵ�ԭ����и�����ӦʽΪ��Fe ��3e��= Fe3+
B. �����������Һ��ͨ������SO2���壺ClO����SO2��H2O �� HClO��HSO
C. ��FeCl3��Һ�м�������С�մ���Һ��Fe3+��3HCO3�� �� Fe(OH)3����3CO2��
D. ���AgNO3��Һ���ܷ�Ӧʽ��4Ag+ + OH�� �� 4Ag+O2+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������H2A��һ��������ˮ�Ķ�Ԫ������NaOH��Һ��������ʵ���Ũ�ȵ�H2A��Һ������Һ��H2A��HA-��A2-�����ʵ�������(a)����ҺpH�ı仯��ϵ��ͼ��ʾ������˵���������

A. ��������H2A![]() HA-+H+�ĵ���ƽ�ⳣ��Ka1=10-3.30
HA-+H+�ĵ���ƽ�ⳣ��Ka1=10-3.30
B. ��c(Na+)=2c(A2-)+c(HA-)ʱ����Һ������
C. pH=6.27ʱ��c(A2-)=c(HA-)>c(H+)>c(OH-)
D. V(NaOH��Һ)��V(HA��Һ)=3��2ʱ��2c(Na+)+c(OH-)=2c(H2A)+c(HA-)+c(H+)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com