
分析 ①CaBr2中只含离子键,为离子化合物;
②金刚石中构成微粒为原子,只含共价键,为原子晶体;
③铜中含金属键,为金属晶体;
④干冰中含共价键,构成微粒为分子,为分子晶体;
⑤Na2SO4中含离子键和共价键,为离子化合物;
⑥碘片中含共价键,构成微粒为分子,为分子晶体;
⑦NH4Cl中含离子键和共价键,为离子化合物;
⑧二氧化硅中构成微粒为原子,只含共价键,为原子晶体,以此来解答.
解答 解:(1)原子晶体熔化时需要破坏共价键,金刚石和晶体硅都属于原子晶体,所以熔化时需要破坏共价键的是②⑧;分子晶体的熔点与其相对分子质量成正比,相对分子质量越小,该分子晶体的熔点越低,干冰和碘都属于分子晶体,二氧化碳的相对分子质量小于碘,所以干冰的沸点最低,故选④;
故答案为:②⑧;④;
(2)溴化钙、硫酸钠、氯化铵中均含离子键,但只含离子键的为①CaBr2,故答案为:①;
(3)属于共价化合物的是④⑧,熔融状态下不导电可证明,故答案为:④⑧;熔融状态下不导电;
(4)晶体中只存在一种微粒间作用力是①(只含离子键)、②⑧(只含共价键),故答案为:①②⑧.
点评 本题考查化学键及晶体中存在的作用力,为高频考点,把握晶体的构成微粒及微粒间的作用力及化学键的判断为解答的关键,注意分子晶体中含分子间作用力,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
| N(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图所示,是原电池的装置图.请回答:
如图所示,是原电池的装置图.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V(C):V(B)=2:3 | |
| B. | 单位时间生成nmolA,同时生成3nmolB | |
| C. | A、B、C的体积分数不再变化 | |
| D. | A、B、C的分子数比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 异戊二烯(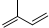 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷(CH3CHClCH2CH3)与NaOH乙醇溶液共热 | |
| C. | 甲苯在一定条件下发生硝化生成一硝基甲苯的反应 | |
| D. | 甲醇在铜催化和加热条件下生成的产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A. | 离子半径大小:Y2->M2->R3+ | |
| B. | Y与M组成的化合物是形成酸雨的原因之一 | |
| C. | 将YM2通入BaCl2溶液中有大量白色沉淀产生 | |
| D. | X的最高价氧化物的水化物碱性大于R最高价氧化物的水化物碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
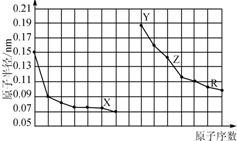
| A. | X、R的最高化合价相同 | |
| B. | 简单离子的半径:X>Y>Z | |
| C. | Y、Z、R对应的最高价氧化物的水化物相互之间可以发生反应 | |
| D. | 电解熔融的X与Z构成的化合物可以得到单质Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com