
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是
A、铜片作原电池的负极,石墨作原电池的正极,氯化钠作电解质溶液
B、铜锌合金在潮湿空气发生电化学腐蚀
C、用铜片作阴、阳电极,电解硫酸钠溶液
D、用铜片作阴、阳电极,电解硫酸铜溶液
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:2017届山东省临沂市高三上学期期中化学试卷(解析版) 题型:选择题
下列有关元素及其化合物的说法正确的是
A.水蒸气通过灼热的铁粉生成氢氧化铁和氢气
B.Mg比Al活泼,更易与NaOH溶液反应生成H2
C.Na在空气中长期放置最终变为Na2CO3粉末
D.向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:选择题
下列事实不能用平衡移动原理解释的是( )
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.工业合成氨时采用铁触媒作反应的催化剂
C.工业生产硫酸的过程中使用过量的空气以提高SO2的转化率
D.将收集NO2气体的烧瓶密闭后放在装有热水的烧杯中,发生颜色变化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的速率
B.NH4HCO3(s)=NH3 (g)+H2O(g)+CO2(g) ΔH=+185.57 kJ·mol-1能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.ΔH<0、ΔS>0的反应在任何温度下都能自发进行
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
关于平衡常数,下列说法正确的是
A.使用催化剂能使化学反应速率加快,平衡常数增大
B.书写相同的反应,平衡常数的数值随温度的改变而改变
C.化学平衡发生移动,平衡常数必发生变化
D.对于3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为

查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A、钢铁发生电化腐蚀的正极反应式:Fe-2e-=Fe2+
B、氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH-
C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+
D、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。下列属于未来新能源标准的是:
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
化学反应的本质是旧键断裂和新键形成的过程,下列关于化学反应叙述错误的是( )
A.放热反应△H < 0,吸热反应△H>0
B.化学键断裂释 放能量,化学键形成吸收能量
放能量,化学键形成吸收能量
C.木炭的燃烧是放热反应
D.吸热反应的生成物总能量大于反应物总能量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷(解析版) 题型:实验题
钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)Al(NO3)3是制备钠硫电池部件的原料之一。由于Al(NO3)3容易吸收环境中的水分,因此需要对其进行定量分析。具体步骤如图所示:
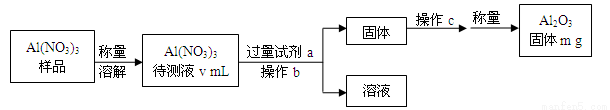
①加入过量氨水后发生反应的离子方程式为:___________________________。
②操作b为:________________。
③Al(NO3)3待测液中,c(Al3+)=___________ mol/L(用含m、V的代数式表示)。
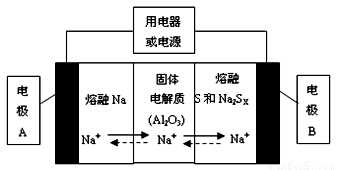
钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050、 |
沸点/℃ | 892 | 444.6 | 2980 |
①根据上右表数据,请你判断该电池工作的适宜应控制在____________(填字母)范围内。
A.100℃以下 B.100~300℃ C.300~350℃ D.350~2050℃
②放电时,电极A为_________极,电极B发生_________反应(填“氧化或还原”)
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:________________。
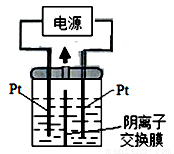
(3)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:________________;试分析左侧溶液蓝色逐渐变浅的可能原因是:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com