
分析 (1)根据C=$\frac{1000ρw%}{M}$和稀释定律C浓V浓=C稀V稀来计算,根据所配制溶液的体积确定容量瓶的规格;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序;
(3)定容方法:向容量瓶中加蒸馏水至液面距刻度线1~2cm,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切;
(4)根据C=$\frac{n}{V}$,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差.
解答 解:(1)浓硫酸的浓度据C=$\frac{1000ρw%}{M}$和稀释定律C浓V浓=C稀V稀=$\frac{1000×1.84×98%}{98}$=18.4mol/L,由于无480mL容量瓶,故应选用500mL容量瓶,配制出500mL1mol/L的稀硫酸,设需要浓硫酸的体积为XmL,根据稀释定律C浓V浓=C稀V稀可知:18.4mol/L×XmL=500mL×1mol/L,解得X=27.2mL,配制450mL 1mol•L-1硫酸溶液需要500mL的容量瓶,故答案为:27.2;500;
(2)根据操作过程是计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶等步骤来排序,可知正确的操作顺序为:⑤④②⑥⑦⑧⑨,故答案为:⑤④②⑥⑦⑧⑨;
(3)定容方法:向容量瓶中加蒸馏水至液面距刻度线1~2cm,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切;如果不小心加多,应该重新配制,故答案为:胶头滴管; 重新配制;
(4)①用以稀释硫酸的烧杯未洗涤,会导致溶质损失,则所配溶液的浓度偏低,故答案为:偏低;
②未经冷却将溶液注入容量瓶中,则冷却后溶液体积偏小,则浓度偏高,故答案为:偏高;
③定容时观察液面俯视会导致溶液体积偏小,则浓度偏高,故答案为:偏高.
点评 本题考查了一定物质的量浓度溶液的配制以及误差分析,难度不大,注意实验的基本操作方法和注意事项.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
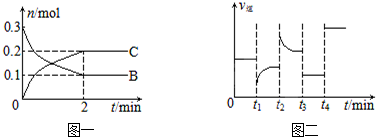
| A. | t2时改变的条件可能是增大c(C),平衡时B的物质的量分数增大 | |
| B. | t1时改变的条件是降温,平衡逆向移动 | |
| C. | t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 | |
| D. | x=2,反应开始2 min内,v(B)=0.1 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
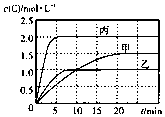 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以表和图表示
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以表和图表示| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5molA 0.5 molB | 1.5 molA 0.5 molB | 6.0 molA 2.0 molB |
| A. | 若平衡时温度不变,改变容器体积平衡不移动 | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | l0min内甲容器中反应的平均速率v(A)=0.025mol•(L•min)-1 | |
| D. | T1℃,起始时甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石蕊,由蓝变红 | B. | 酚酞,红色褪去 | C. | 甲基橙,由黄变橙 | D. | 甲基橙,由橙变黄 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与酸反应产生氢气多 | B. | 与碱反应产生氢气多 | ||
| C. | 一样多 | D. | 不知道铝粉的质量,无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入22.4LSO2参加反应时,有2 NA个电子发生转移 | |
| B. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| C. | 滴加KI溶液时,KI被氧化,CuI是氧化产物 | |
| D. | 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
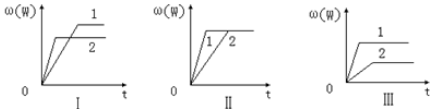
| A. | 图Ⅰ可能是不同压强对反应的影响,且P2>P1,m+n<p | |
| B. | 图Ⅱ可能是不同压强对反应的影响,且P1>P2,m+n=p | |
| C. | 图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0 | |
| D. | 若m+n<p,△H>0,则该反应在低温下容易自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ③和④ | C. | ②和③ | D. | 只有③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com